引言
分子的柔性对于药物的ADMET性质具有重要影响,因此在药物发现的早期,常常利用分子的柔性作为过滤规则对大规模化合物库进行筛选,柔性太大的分子被认为不会作用于传统的药物靶点。然而,近年来研究发现,对于一些不能被符合传统类药五规则化合物调控的特殊靶点,分子量、柔性较大的分子成为这类靶点的研究热点。因此,如何定量描述化合物的柔性成为关键,本文介绍了三种最常用的描述化合物柔性的描述符,并讨论了相应的应用特征。

现代药物的发现需要柔性描述
最近的研究表明,尽管一些化合物不符合类药性五规则(Ro5),称为类药五规则化学空间之外(bRo5),但它们仍然在药物发现过程中取得了成功。鉴于这些化合物能调控具有难结合位点的蛋白靶点,这引起了药物化学家的极大兴趣。过去一些文章报道了相关的研究,其中分子量(MW)、氢键供体(HBD)、氢键受体(HBA)、拓扑极性表面积(TPSA)、油水分配系数(cLogP或cLogD)、可旋转键(NRot)等是这些研究中广泛应用的参数。最近,Schultz指出,针对新的化学空间,应该避免过度简化一些筛选规则,例如,TPSA不是一个很好的过滤描述符,因为它高估了极性。在先前的论文中,还讨论了需要更新分子特性,来考虑大分子和柔性候选药物的特殊特征,评估bRo5化学空间中的极性、分子内氢键(IHHBs)和亲脂性描述符。到目前为止,分子的柔性在早期药物发现中的作用还没有明确讨论。Veber和合作者首次揭示了柔性对吸收、分配、代谢和排泄(ADME)性质的作用,他们认为分子柔性、极性表面积和氢键数是生物利用度的关键决定因素,Varma等人也得到了类似的结果。
柔性描述符在大多数制药指标中得以应用。然而,需要注意,对于构象依赖的物理化学性质,柔性分子将表现出不同的值。例如,两个构象的亲脂性可能有显著差异。分子变色龙的鉴定,CsA(即柔性化合物会根据周围环境改变自身性质)进一步支持这一假设。亲脂性和极性的实验值,预期代表最相关构象者所取的平均性质值。当使用亲脂性和极性的实验值时,因此,当使用亲脂性和极性的实验值时,也隐含地应用了作为口服候选过滤的柔性。其次,柔性会导致分子特性的变异,不仅会影响药物的药代动力学(PK),而且还会影响药物和候选药物的药效学(PD)。
最常见的柔性描述符:可旋转键数目NRot
分子柔性主要与分子中单键的存在有关,通常是sp3杂化的C-C键。原子在单个键周围的“自由”旋转允许分子采用不同的构象,当单键的数目增加时,柔性也增加。虽然药物发现的柔性的概念和相关性已经确立,但由于缺乏直接的实验手段,因此将其转化为定量描述符是困难的。因而,阻止了对描述符的性能进行任何持续的评估。核磁共振(NMR)可以在溶液中提供实验构象,但这只是一种间接的柔性度量。获得柔性指数的一种常用方法是从分子的2D结构开始并计数NRot。Veber把一个可旋转的键定义为一个非末端重原子(即非氢原子)上的任何单键,并且不在环中,酰胺C-N键由于其高旋转能垒而被排除在计数之外。NRot是一个离散值,可以很容易地由大多数分子模拟软件包计算,自2002年以来,它被用于许多研究,以强调药物发现柔性的相关性。
NRot存在的问题
尽管NRot被广泛使用,但在某些情况下可能会有问题。首先,NRot忽略了环部分的柔性。例如,正十二烷(图1a)具有NRot=9,而其环类似物(图1b)NRot=0。大家可能认为环部分常常假设一种预先形成的构象,因此,它们对分子的总柔性没有贡献。DOTA的复合物被用来讨论这一点。DOTA(图1c,e)是一种大环配体用于磁共振成像(MRI)中注入镧系钆(III)离子。自由DOTA的晶体结构(图1c)显示了类似于镧系化合物中的大环构象(图1d)。这一证据可能表明,当复合物形成时,大环并没有改变其构象。然而,对一系列镧系DOTA配合物(LnDOTA)进行的大量核磁共振和模拟研究表明,DOTA大环存在构象变化(图1f)。总的来说,这些实验结果证实,环部分对分子的整体柔性是有贡献的。
NRot的另一个缺点是它的离散性。图2显示了东莨菪碱、丙戊酸、胆固醇和ZINC100907004。尽管它们的化学结构有很大的差异,这四种化合物具有相同的NRot值。例如,丙戊酸是脂肪族的,而胆固醇有多环;东莨菪碱含有托烷部分,ZINC100907004有两个脂肪族环。其次,NRot既不能区分立体异构体,也不能区分区域异构体(即,一类具有相同官能团但连接在不同位置的组成异构体),而立体和区域异构体的柔性可能是不同的 。图2显示了两个非对映异构体,化合物1和5,两种异构体的NRot=10,但一系列实验测定表明,1形成IMHB,这降低了柔性。因此,1显示出与5显著不同的溶解度和渗透性特性。图2还显示了两个区域异构体(化合物11和12)。辉瑞公司的研究人员实验表明,12可以形成IMHB,因此,具有比11低的柔性。
柔性指数Φ
Kier在1989提出的柔性指数Φ。Φ是一个拓扑指数(使用分子图计算),它定义了基于结构属性的分子柔度,从而减轻归因于无限柔性分子的值, 根据它的定义Φ是一个连续值。一个完全柔性的分子被假定为一个由sp3杂化的C原子(Csp3)组成的无止原子链。缓解这种情况的结构特征是:(i)更少的原子;(ii)环的存在;(iii)分支的存在;(iv)共价半径小于Csp3的原子的存在。
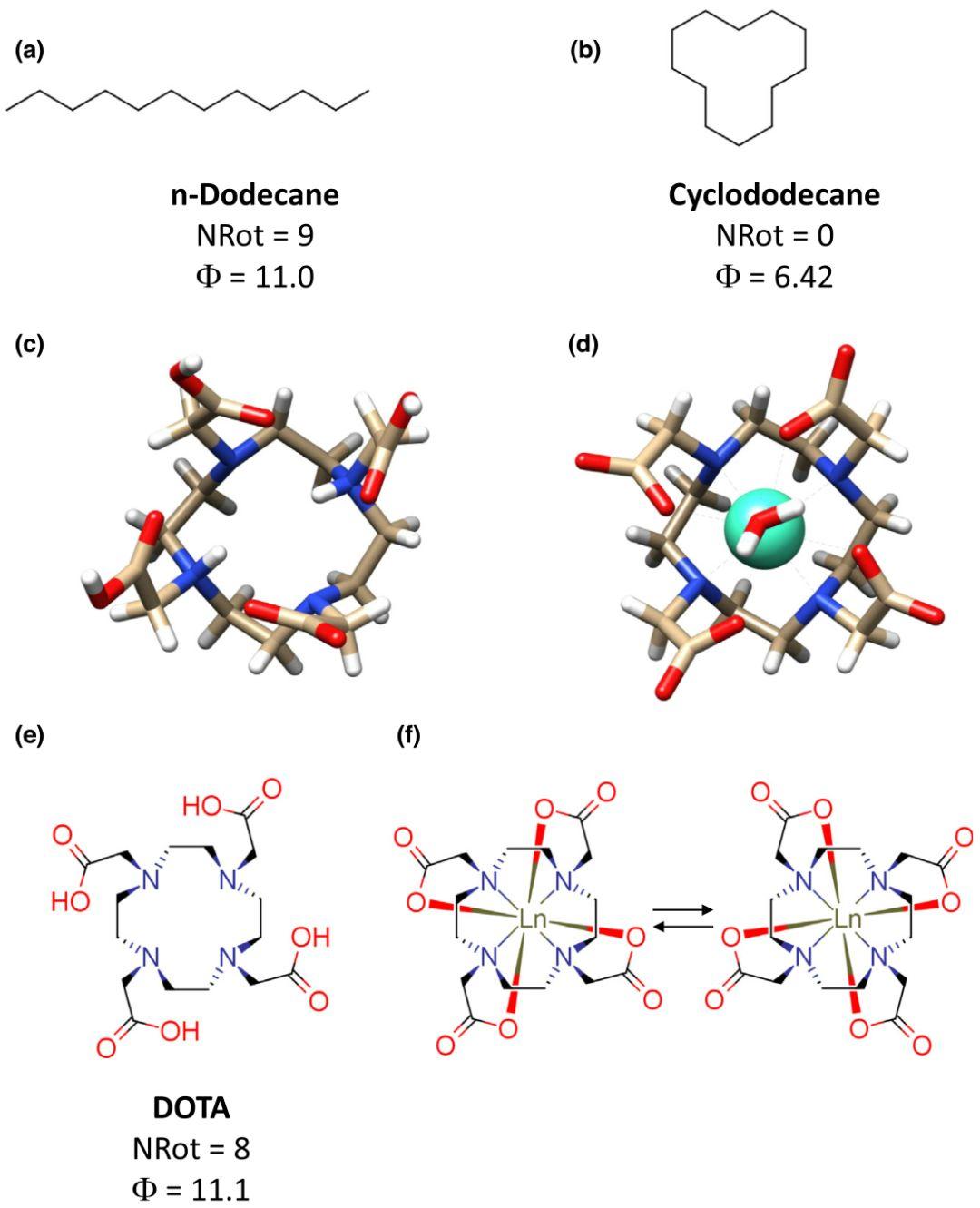
图1.比较NRot和Φ提及的化合物结构
图片来源:Drug Discov Today
Φ能否取代NRot在早期药物发现中的作用?
在图1b中,Φ=6.42,而NRot=0。这个Φ值低于对应的线性分子(Φ=11.00,图1a)。换句话说,Φ可以获取环状化合物可以是柔性的,尽管小于它们相应的线性类似物。如前所述,Φ可以假定连续值。在图2a-d中,对于NRot=5的四种化合物,Φ的范围从3.54到8.15。丙戊酸和胆固醇显示出相似的Φ值。胆固醇的柔性来自于侧链,其包含五个sp3原子。这个例子阐明了NRot如何捕捉到分子中与环状部分相连链的柔韧性,而Φ可能是整个分子柔韧性的较好描述符。对于东莨菪碱(图2a),Φ小于NRot,这是因为结构的基序对分子柔性(例如,Csp2原子)不利。此外,由于Φ是一个连续变量,它在定量结构-属性关系(QSPR)建模中的应用应该是首选的。最后,图2e -h显示,由于其2D性质,Φ(类似于NRot)也不能区分立体和区域异构体的柔性。
3D描述符nConf20
鉴于3D描述符的复杂性,不适合作为早期药物发现的度量。然而,现代计算机体系结构的自动化和不断增强的处理能力有助于获得建模工具进行计算。因此,本文讨论了3D柔性描述符在早期药物发现中的潜力。一般来说,构象的数目越多,化合物柔性就越大。Wikor和Cooper提出了一个基于3D构象的柔性指数nConf20。在这种方法中,SMILES被用来生成所研究分子的50个随机分子构象。使用MMFF94力场对每个构象最小化。每个构象及其相对于找到的最低能量构象的能量都被保留下来。nConf20是能量相对于最低能量构象<20 kcal/mol的构象数(不包括最低能量构象) 。该方法作为Python脚本免费提供,并成功地用于预测有机分子的结晶倾向。
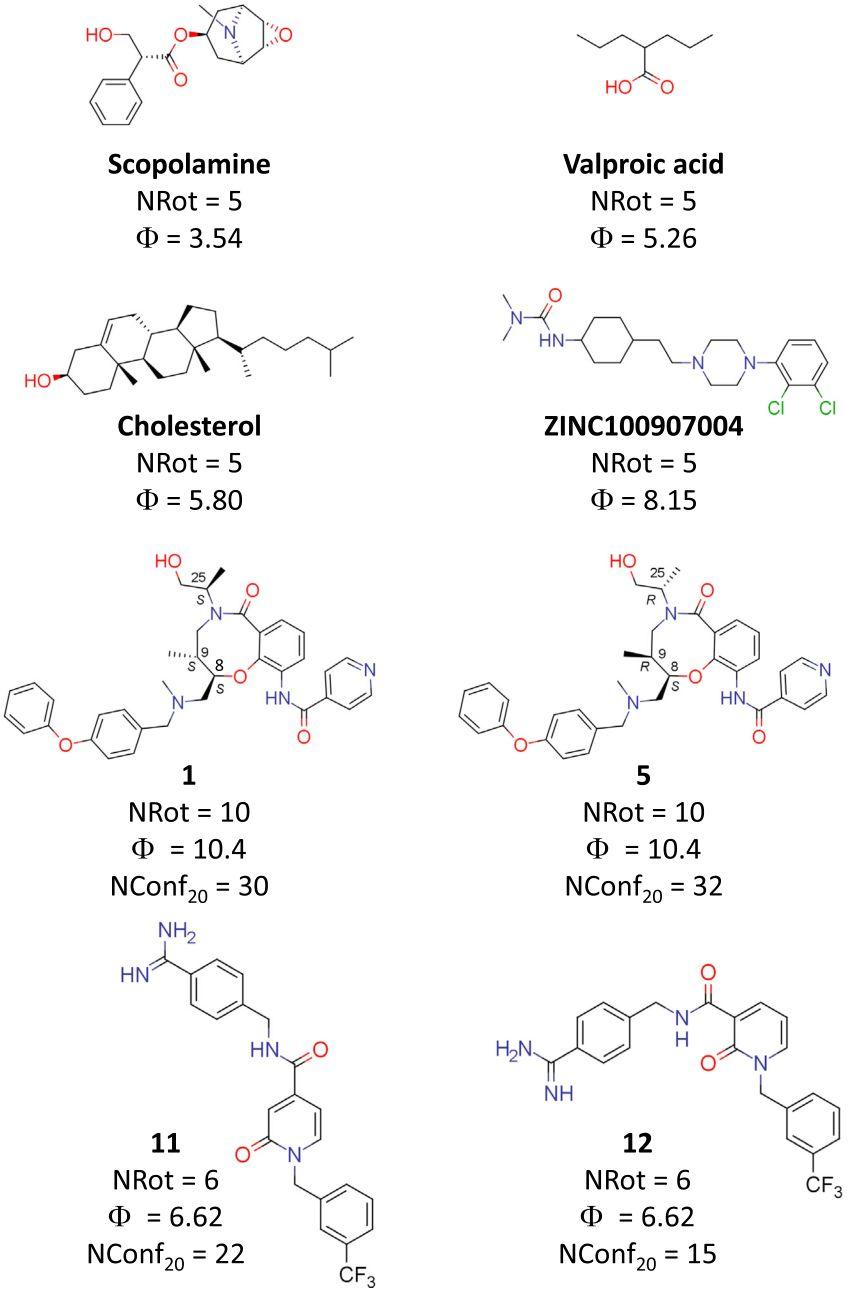
图2. 讨论柔性指标所涉及的化合物结构
图片来源:Drug Discov Today
值得注意的是,对于图2中的立体异构体1和5,nConf20分别为30和32。所揭示的这种柔性差异可能是两种异构体的不同亲脂性和渗透性的原因。nConf20还可区分区域异构体的柔性(图 2 中化合物 11 和 12)。由于nConf20是最近才引入的,因此很难对其价值进行评估。并且,还没有定义一种对所有化合物都有效的通用构象取样策略。特别是,众所周知的大环之类的化合物需要特定的计算工具,因此,至少对于大环和复杂结构而言,使用MMFF94作为计算能量的方法和20 kcal/mol作为能量阈值还是被质疑的。加上缺乏能够验证计算策略的实验值,目前不鼓励在早期药物发现中使用 3D 柔性描述符。
bRo5化学空间的柔性判断
如前所述,分子柔性影响在bRo5化学空间中至关重要。环肽(CPs)是一类bRo5类化合物,具有可调控的结合多种靶分子的能力,为新型药物的开发提供了良好的骨架。
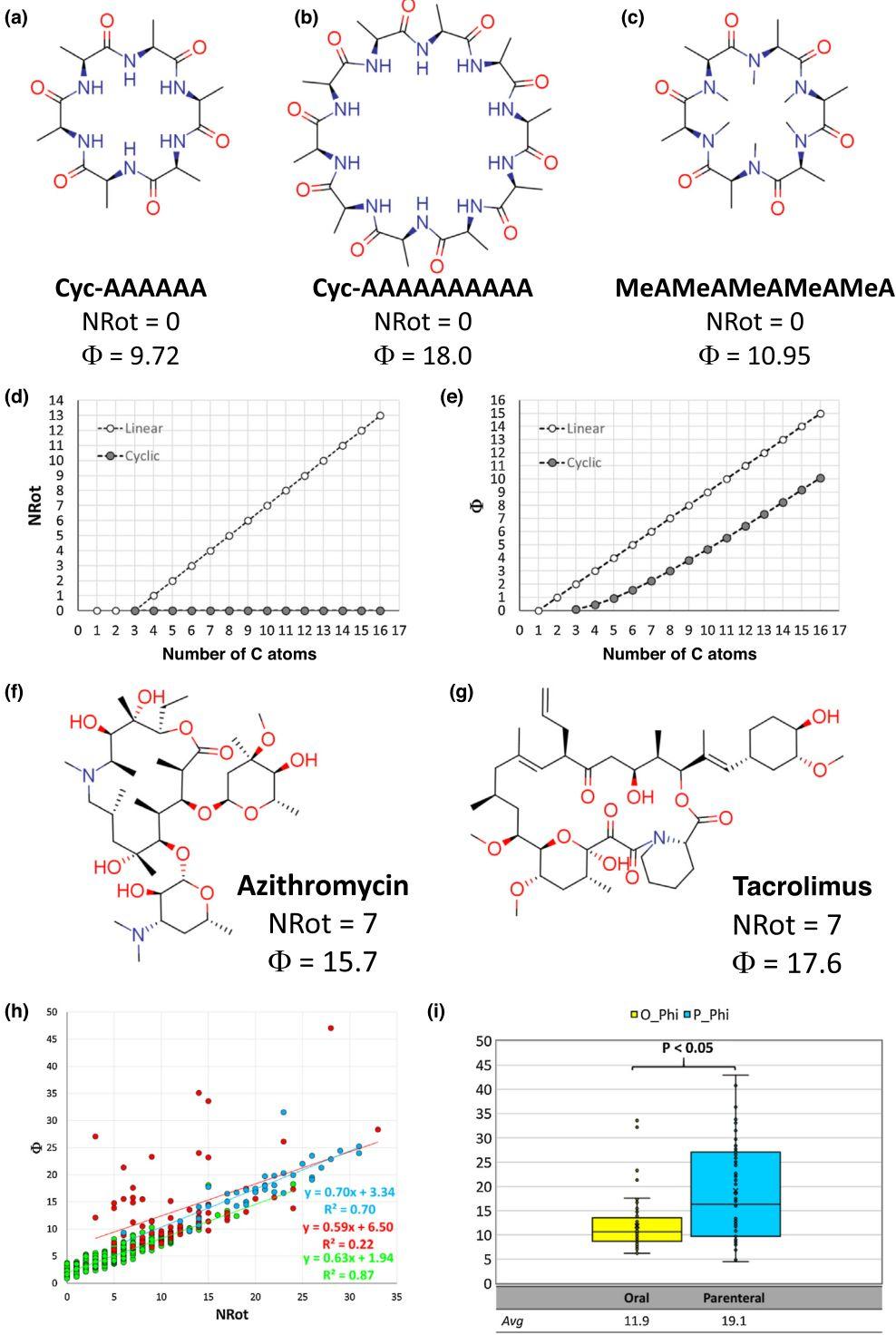
图3. Φ和NRot的比较
图片来源:Drug Discov Today
目前,已经报道了几种不同大小和柔性的CPs化合物。这里建议用Φ而不是NRot来比较不同大小CPs的柔性。图3a、b中展示了两种含丙氨酸的环肽(六肽和十肽)及其柔性指数。值得注意的是,两个分子的NRot都为0,而Φ分别为9.72和18。为了推广这一概念,图3d显示了NRot的趋势, NRot不能评估循环结构比线性结构更不灵活。Φ(图3e)的趋势在某种程度上反映了一种直观的观察,即环结构(灰色圆圈)比线性结构(白色圆圈)柔性更低,但在某一点之后,柔性几乎以同样的方式增加。除了环化,NRot不能监测环肽柔性的变化,如图3c中的N-甲基化环六肽所示,其NRot=0,与图3a中的非甲基化类似物相同;相反,由于N-甲基化,Φ的增加已被证实。然而,这个结果是有疑问的,因为主链酰胺的N-甲基化不会导致更灵活的分子。大环是第二类重要的bRo5化合物,难以用NRot处理。例如,阿奇霉素和他克莫司(图3f,g)具有相同的NRot,但Φ不同(分别为15.7和17.6)。正如其他文献所指出的,与阿奇霉素相比,对现有晶体结构的分析支持他克莫司具有更大的柔性,这可能与大环的大小有关。
总的来说,NRot限制可能会影响回顾性研究。图3h显示了NRot和Φ之间的关系如何随数据集而变化。首先,作者从Schultz的论文中提取出673种符合Ro5的药物(绿点)。对于这些化合物,NRot和Φ之间的关系是线性的,并且非常显著(R2=0.87)。随后,作者收集了来自同一篇论文中75种bRo5化合物(红点)。在这种情况下,NRot和Φ之间的关系很差(R2=0.22)。这一发现与所研究的bRo5数据集中存在的许多大环结构一致。最后,作者使用了Edmondson和同事最近发表的38个蛋白水解靶向嵌合体(PROTACs)的数据集(浅蓝色点)。监测柔性对于PROTACs尤其重要,因为最近的研究表明,在链接区中引入刚性片段是有益。对于PROTACs,NRot和Φ之间的关系是显著的(R2=0.70)。这与PROTACs通常是非大环且强柔性的结构的证据是一致的。
以Φ表示分子柔性可能是一个很有前途的工具,可以用来生成候选药物的排名指标。例如,来自DeGoey等人的论文, 作者收集了两组bRo5化合物:第一组包括69种口服化合物,第二组67种非口服药物。对于这两个数据集,分别计算了Φ值。图3i显示了所调查的bRo5药物给药途径与Φ的箱体图。口服药物的Φ范围明显小于非口服药物。虽然很少有胃肠外药物显示出低Φ值,但有理由假设bRo5化合物靶向占据Φ<11.9,将提高可达到合理口服吸收水平的几率。
总结
柔性影响口服生物利用度,在早期药物发现过程中,通常由NRot进行量化。不符合Ro5的大分子和柔性分子(bRo5)作为候选药物变得越来越有吸引力。然而,标准分子描述符从Ro5转移到bRo5化合物并不是自动的。使用时不仅要注意亲脂性和极性,还要注意柔性指标。 在选择合适分子的描述符时,可以参考一下几点:
Ø NRot 和Φ是适用于早期药物发现的柔性指标。
Ø 在存在环结构的情况下 ,应首选Φ 。
Ø Φ与NRot都不能区分立体和区域异构体的柔性,nConf20可以。
Ø nConf20依赖于构象采样方法和能量阈值,暂时缺乏相应标准,对于大环和复杂结构而言不太合适。
参考文献:
Caron, G. et al. Flexibility in early drug discovery: focus on the beyond-Rule-of-5 chemical space, Drug Discov Today (2020), https://doi.org/10.1016/j.drudis.2020.01.012