先睹为快
靶点
羧酸酯酶carboxylesterase(LαE7)PDB ID:4FNG
筛选化合物库
23,000硼酸类市售化合物的分子库
计算方法
共价虚拟筛选(Covalent Virtual Screen)
计算软件
DOCK3.6(http://covalent.docking.org/)
单位与作者信息
澳大利亚国立大学的Colin J. Jackson教授,
魏茨曼科学研究所的Nir London教授
发表杂志
The Proceedings of the National Academy of Sciences
计算流程
本文作者用共价抑制剂筛选的DOCKovalent算法,针对LcαE7的蛋白晶体结构筛选了23000硼酸分子库。手动检查对接结果中排名前500(top2%)的结合模式,最终,综合直觉、价格和商业用途等因素挑选出5个候选化合物, 实验测试均为nM级别。
背景介绍
随着世界人口的增加,农业生产力对维持粮食安全至关重要。杀虫剂可以控制农业害虫和病媒,进而保障了全球粮食安全和健康。就全球健康而言,杀虫剂是抵御许多传染病的第一道防线;在发展中国家,杀虫剂尤其重要,因为在发展中国家,昆虫传播媒介占所有传染病的近20%,然而,杀虫剂的广泛使用已经选择出了具有抗药性的昆虫。自20世纪40年代以来,报告抗药性的昆虫种类迅速增加,已超过580种。抗药性使杀虫剂失效,导致了杀虫剂使用量的增加,对环境造成了严重的影响。抗药性广泛存在,已然成为紧迫的全球性问题。有机磷酸酯Organophosphates和氨基甲酸酯carbamates是目前使用最广泛的两类杀虫剂。它们通过对亲核活性位点的丝氨酸残基磷酸化/氨甲酰化,来抑制胆碱能神经肌肉连接处的乙酰胆碱酯酶(AChE),导致乙酰胆碱在生物体内不断积累,最终导致其无休止的神经信号传导和死亡。对有机磷农药(OPs)等杀虫剂的抗性通常涉及羧酸酯酶carboxylesterases (CEs)对OPs的分离或水解。克服抗药性主要集于开发具有新的作用方式的新型杀虫剂,尽管这些新靶点中有许多显示出希望,但生物化学靶点的数量有限,而且新靶点对靶点不敏感和代谢抵抗的问题也不可避免。既然,杀虫剂的抗性通常涉及羧酸酯酶,抑制羧酸酯酶是可以恢复已形成抗性的OPs的有效性。这种通过抑制杀虫剂抗性所涉及的酶来提高杀虫剂的效力(增效剂)的最突出的一个案例就是胡椒基丁醇,可用于增强氨基甲酸酯类和拟除虫菊酯的活性。

增效剂的概念可以进一步具体地针对已经进化成具有代谢抗性的酶,从而将杀虫剂的功效恢复到抗药性前的水平。因此,可以针对杀虫剂抗性的理想靶标羧酸酯酶,如LcαE7,设计消除抗药性的抑制剂(图1)。LcαE7通过典型丝氨酸水解酶机制催化脂肪酸底物的水解。已知硼酸与丝氨酸水解酶的丝氨酸形成可逆共价加合物,其模拟了羧酸酯水解的过渡态几何结构,因此具有高亲和力。
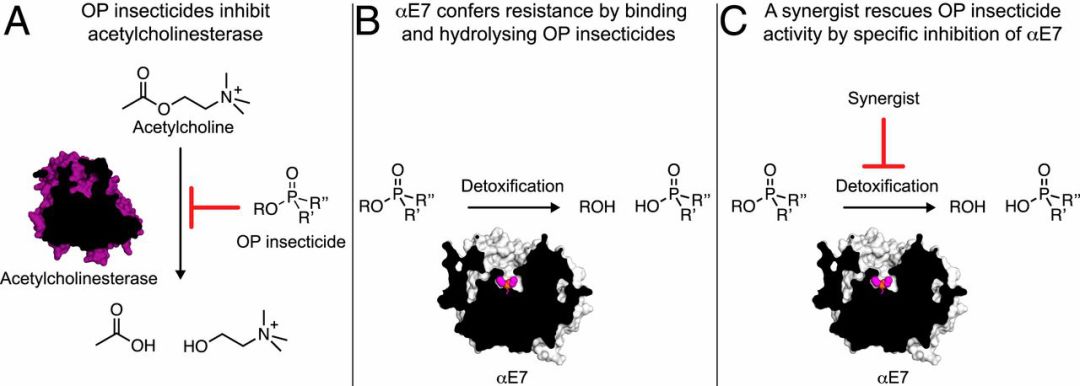
图1. 有机磷杀虫剂OPs增敏剂概述
图片来源PNAS
计算方法和结果部分
本文作者使用DOCK3.6软件里面的共价抑制剂虚拟筛选的通用方法DOCKovalent算法(http://covalent.docking.org/),针对LcαE7的蛋白晶体结构(PDB 编号:4FNG)筛选了23,000硼酸类市售化合物的分子库,手动检查对接结果中排名前500(top2%)的结合模式,最终,综合直觉、价格和商业用途等因素挑选出5个候选化合物。
蛋白的前处理时将关键残基Ser218设置为去质子化状态,His471设为双质子化状态;在配体准备过程中,由于无法参数化B原子,用C原子取代,这种替换并不会影响打分结果。共价对接中将形成的B-Oγ键长设为1.5 ± 0.1 Å,键角Cβ-Oγ-B = 116.0 ± 5° 和 Oγ-B-R(Ligatom)=109.5±5°。并且在测试化合物的手动选择中,优先选择硼酸的羟基占据氧阴离子孔(由Gly136、Gly137和Ala219的主链氮形成)(图2)。
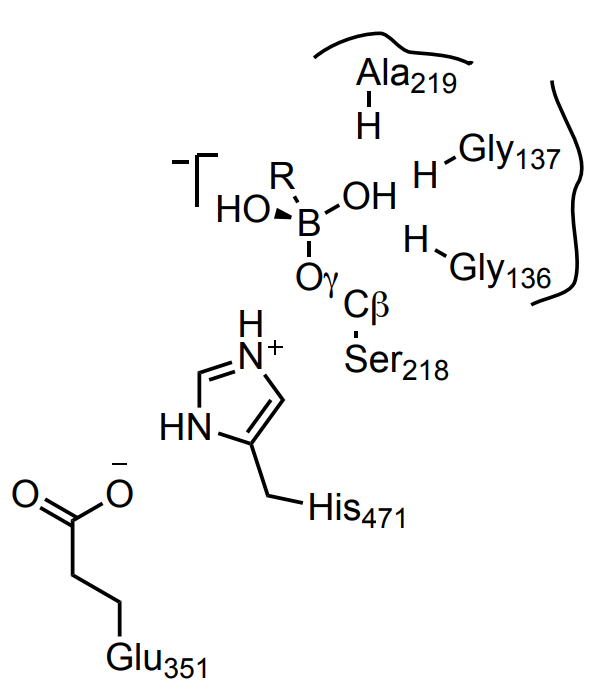
图2. 虚拟筛选过程中硼酸分子与LcαE7酶Ser218残基配位模式
图片来源PNAS
筛选的5种化合物都有一个苯基硼酸(PBA)亚结构。作者解决了LcαE7酶与化合物1-5的共晶结构(图3-紫色棍棒结构),很大程度上验证DOCKovalent预测的对接模式(图3-黄色棍棒结构)。筛选的5个硼酸化合物对野生型 LcαE7酶的Ki值均低于12 nm,其中最强的化合物3的Ki值为250 pm。对于突变型Gly137Asp LcαE7酶而言,化合物2的抑制活性表现最好(Ki=29nM)。
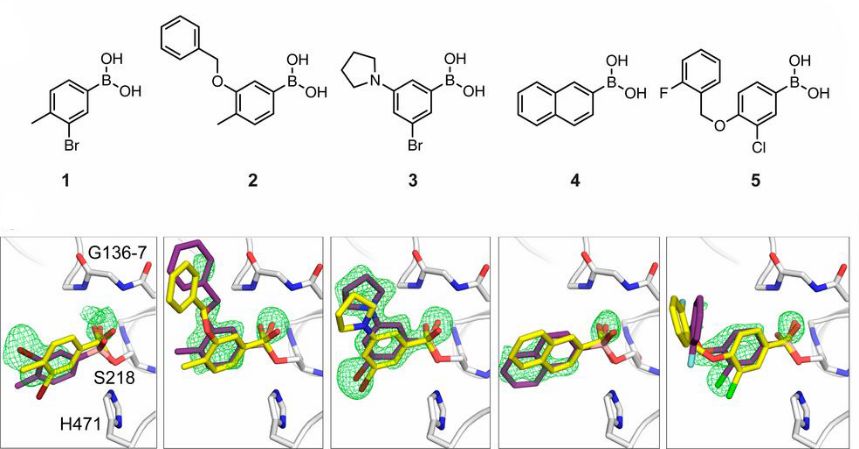
图3. 共价对接预测的lcαe7的有效抑制剂的化学结构和复合物共晶结构
图片来源PNAS
为了在保持良好的野生型效价同时提高对突变体gly137asp的抑制作用,作者基于构效关系的研究,进一步优化了抑制剂的结构,得到了目标化合物3.9和3.10,并结晶了3.10抑制剂和突变体Gly137Asp LcαE7酶的共晶体(图4)。
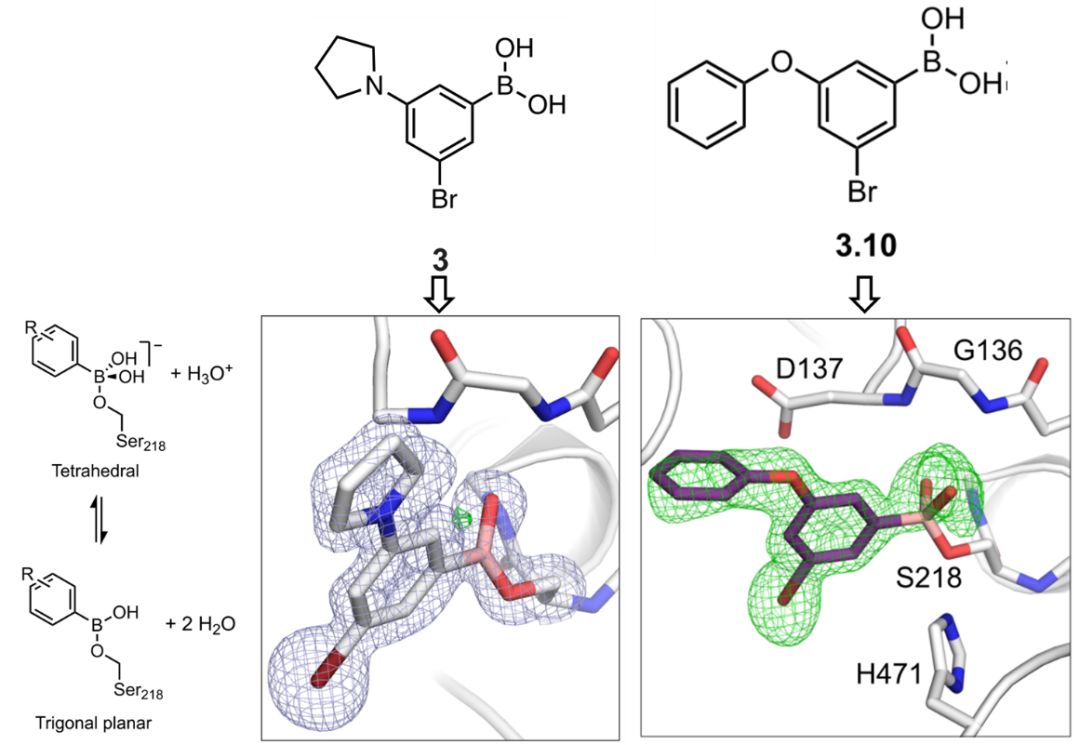
图4. 化合物3和3.10的化学结构式和复合物的结合模式图
图片来源PNAS
与抑制剂3相比,发现3.10的取向更加保守,3-溴取代基与活性中心高度互补,5-苯氧基取代基朝向活性中心的狭窄空间,避免了与Asp137侧链的立体位阻。最令人惊讶的是,化合物3.10采用的是四面体几何结构,而不是化合物3观察到的三角平面几何结构。四面体硼酸化合物与丝氨酸水解酶的亲和力结合更高,这也进一步解释了3.10化合物在活性上高于3化合物6.1倍。
进一步的药理实验证明,这类化合物可以选择性作用于LcαE7,在高剂量下对哺乳动物无害;通过对蝇蛆菌株的测试结果显示,LcαE7酶抑制剂可以作为增效剂来恢复OPs杀虫剂的药效;并且在毒死桃-马铃薯蚜虫中也起到了协同作用,这表明硼酸类LcαE7酶抑制剂具有广谱杀虫剂增效剂的潜力(图5)。
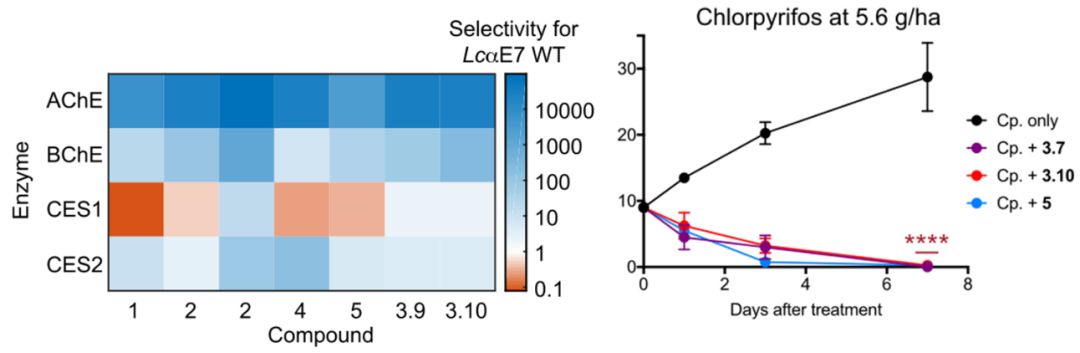
图5. 硼酸化合物的酶选择性验证和OPs杀虫剂协同作用实验
图片来源PNAS
总结
本文报道1了一种利用计算设计高效特异性的LcαE7酶抑制剂。利用DOCKo -valent算法,基于靶点LcαE7酶结合口袋的Ser218的共价作用模式,对23000硼酸数据库搜索,得到了一系列的共价小分子化合物,再结合构效关系的研究,发现了活性更佳的先导化合物。这些化合物逆转了两种不同害虫的抗药性,可以在不影响药效的情况下大幅度减少杀虫剂的使用,可产生重大的经济和环境效益。
DOCKovalent算法是由Nir London教授2等人开发的一种高通量共价虚拟筛选的在线服务型数据库(http://covalent.docking.org)。DOCKovalent数据库包含了不同类型的亲电化合物,包含了醛类,硼酸类,氰基丙烯酰胺类等;并且大多配体的立体结构及构型都是事先准备好的,所以很适合研究者对感兴趣的靶点进行快速的共价对接,打分函数主要评价配体和受体的范德华力和亲电相互作用,并根据打分结果进行排序。
参考文献:
1. Correy, G. J.; Zaidman, D.; Harmelin, A.; Carvalho, S.; Mabbitt, P. D.; Calaora, V.; James, P. J.; Kotze, A. C.; Jackson, C. J.; London, N., Overcoming insecticide resistance through computational inhibitor design. Proceedings of the National Academy of Sciences 2019, 201909130.
2. London, N.; Miller, R. M.; Krishnan, S.; Uchida, K.; Irwin, J. J.; Eidam, O.; Gibold, L.; Cimermančič, P.; Bonnet, R.; Shoichet, B. K., Covalent docking of large libraries for the discovery of chemical probes. Nature chemical biology 2014, 10 (12), 1066.