先睹为快
靶点
FLAP:5-脂氧合酶激活蛋白(PDB ID:2Q7M)
数据库
Molport数据库(6255980个小分子)
ChEMBL数据库(267个已知FLAP抑制剂分子)
计算方法
分子对接
药效团
化学多样性聚类
随机森林方法
分子动力学模拟
计算软件
Schrödinger Suite、Canvas、KNIME、Desmond、Gromacs
计算流程
作者结合基于结构和配体的组合策略建立多步骤虚拟筛选流程,依次通过分子对接、药效团过滤、化学多样性聚类分析、3D-QSAR和随机森林法筛选、目视筛选等方法,筛选了Molport库中约62万个小分子,选出了20个化合物进行生物活性测试以及分子动力学模拟,20个分子中有12个在10μM时具有生物活性,其中4个分子的IC50值<1μM。本研究建立的多步骤虚拟筛选方法提高了阳性分子的命中率,筛选的HIT分子与已知的FLAP抑制剂相比,具有明显不同的化学类型,可作为开发新型FLAP抑制剂的先导化合物。

虚拟筛选流程
作者结合基于结构和配体的方法建立新型多步骤虚拟筛选流程发现潜在的FLAP抑制剂。具体筛选流程如下(图1):
分子对接:对接6255980个分子,保留得分小于-6.00的小分子;
药效团过滤:剩余的4640523个分子使用药效团进行过滤;
化学多样性聚类:通过化学差异和聚类对剩余的359497个分子进行选择;
3D-QSAR和随机森林方法:通过药效团比对评分、三维定量结构定量构效关系(3D-QSAR)模型和随机森林方法对剩余的20000个分子进行评估,根据其预测的活性类别对抑制剂分子进行分类;
目视筛选:对剩余的1000个分子进行深度目视检查,并选择100个具有所需结合轮廓的配体;
根据新颖性、可获得性和化学多样性,最终获得了20个分子;
分子动力学模拟:使用分子动力学模拟进一步评估所选分子的结合性质。
分子对接
作者评估了活性化合物是否可以在诱饵化合物产生的结合分数的分布方面表现出更好的结合分数。分析表明,有效抑制剂(IC50或Ki值<1μM)的对接分数均小于−6,该值被设定为虚拟筛选中的第一过滤器。总共,6255980个来自Molport的化合物被对接到的FLAP的结合位点中,通过表征配体−蛋白结合的相互作用能对化合物进行排序。在这一轮虚拟筛选中,筛选出的分子数量为4640523个。
药效团过滤
作者以已有的FLAP抑制剂分子构建了4个具有相似药效团特征但具有不同3D构象排列的药效团模型,这4个模型被用于分子对接后产生的小分子结合姿势的进一步过滤。这一策略的目的是成功地覆盖属于不同化学簇的所有有效的FLAP抑制剂,这些化学簇具有不同的结合模式。最终保留了359497个独特的分子。
化学多样性聚类
用Canvas软件计算剩余359497个小分子四点药效团的指纹图谱,化合物根据其多样性使用相同的软件包进行聚类,分成了100个簇。然后考虑化学多样性并进行目视检查选择了其中20个簇总共20000个小分子进入下一步筛选。
3D-QSAR和随机森林方法
由于对接得分的预测能力较低,作者使用已知的FLAP抑制剂进行3D-QSAR建模,以提高计算模型对虚拟筛选研究的预测能力。作者基于56个训练集分子与9个测试集分子构建了比较分子相似指数分析(CoMSIA)模型(图2)。使用Canvas计算ChEMBL数据库中的267种FLAP抑制剂的物理化学和拓扑描述符,在生成的数据集的基础上,用KNIME程序应用随机森林方法。然后,根据药效团比对得分、CoMSIA模型和随机森林方法对上步的20000个分子集进行筛选。结果,这些分子被进一步分类为预测的活性/非活性化合物两种类别,筛选获得了1000个分子。
目视筛选
肉眼观察1000个分子在结合口袋内的姿势与结合方式,以选择最佳的100个配体,使配体−蛋白与残基H28,D62,Y112,K116和F123发生有利的相互作用。在这些化合物中,考虑到现有技术、合成可行性和化学多样性标准,精心挑选了20个小分子进行生物筛选(图3)。
分子动力学模拟
作者首先运行了10ns的分子动力学模拟,20个小分子均具备稳定的结合模式,随后对这20个分子进行了生物活性测试,生物测试中最活跃的四个分子的为化合物4、11、16和20。之后将分子动力学模拟延长至100ns。100ns运行的结果与10ns的模拟结果相似,且这20个分子的占有值与作者课题组以前发表的分子的结合性质相似。在结合模式上,化合物4(图4A)的羧酸盐阴离子与H28形成水桥,与K116形成盐桥,该分子的N-苄基与F123产生π−π相互作用。化合物11(图4B)显示硝基与H28形成氢键,咪唑环的第三个氮原子与Y112形成水桥,该分子的2-(三氟甲基)苯基与F123产生π−π相互作用。化合物16(图4C)的甲氧基苯基部分与H28形成水桥,噻吩和三唑片段与F123产生π−π相互作用。对称化合物20(图4D)的苯胺中的一个与H28形成π−π相互作用,另一个苯胺基团与D62形成氢键和水桥,D62位于活性中心的内部疏水口袋中。
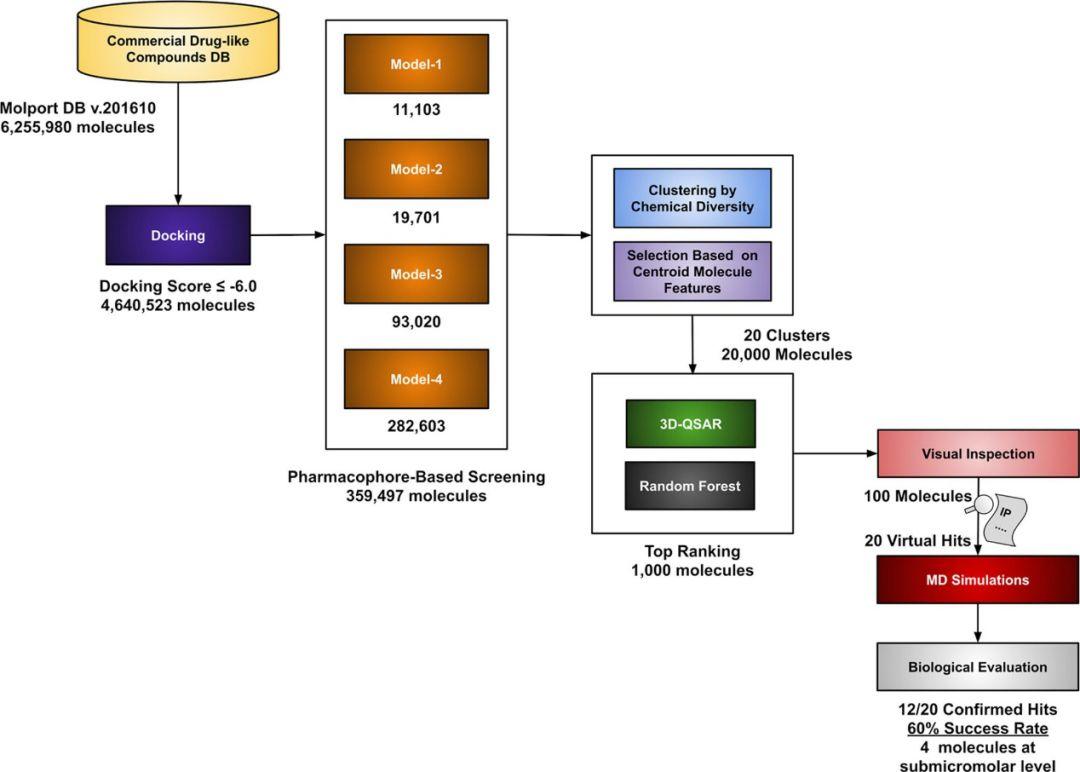
图1.虚拟筛选发现新型FLAP抑制剂的工作流程
图片来源JCIM
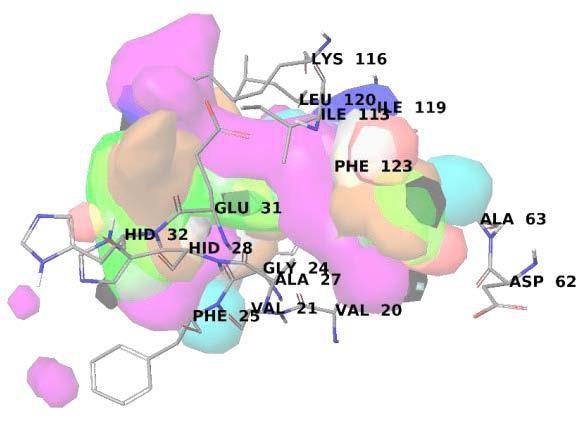
图2.CoMSIA模型显示在FLAP结合部位
图片来源JCIM
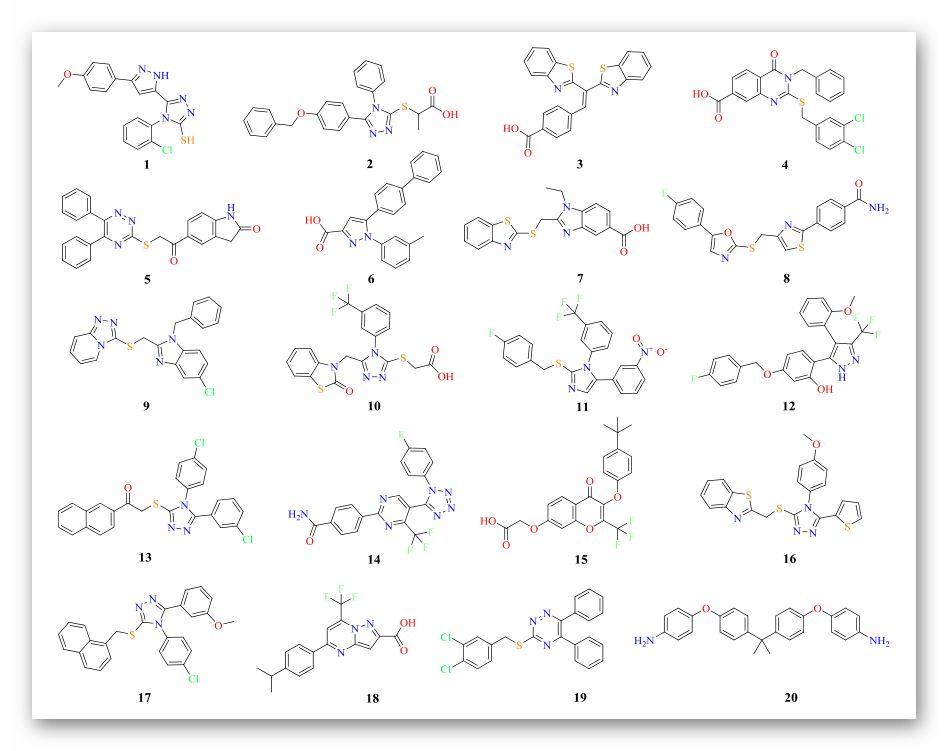
图3.命中的20个小分子的化学结构
图片来源JCIM
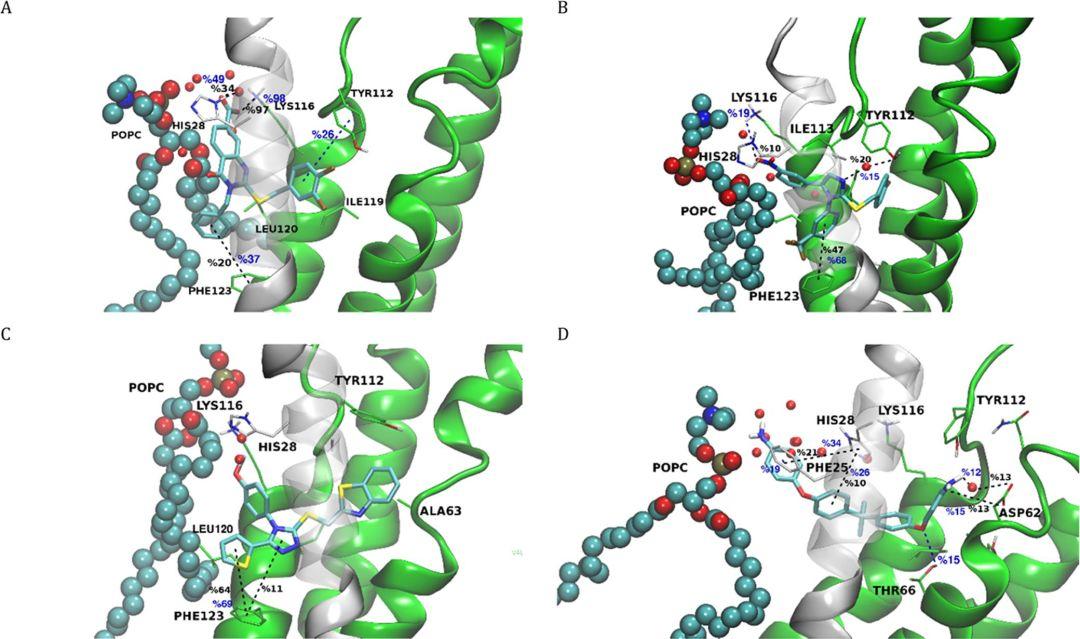
图4.化合物(A)4、(B)11、(C)16和(D)20的分子动力学模拟分析
图片来源JCIM
参考文献:
Olgac A, Carotti A, Kretzer C, et al. Discovery of novel 5-lipoxygenase-activating protein (FLAP) inhibitors by exploiting a multistep virtual screening protocol[J]. Journal of Chemical Information and Modeling, 2020. DOI: 10.1021/acs.jcim.9b00941