药物发现的目的是为了寻找具有特定化学特征的新型化合物,这些化合物可以作为先导化合物进一步研究。高通量虚拟筛选(High-throughput Virtual Screening,HTVS)已被证明是一种有前景且资源有效的先导化合物开发工具,为了说明HTVS对制药行业新型化学系列挖掘的积极影响,美国Janssen 公司总结了3个应用高通量虚拟筛选方法加速先导化合物开发的研究案例,于2月份发表在JCIM杂志上。这3个前瞻性案例的研究靶标分别是Bruton Tyrosine Kinase (BTK)、RAR-Related Orphan Receptor γ t (ROR γ t)和Human Leukocyte Antigen DR isotype (HLA-DR)。前面为我们介绍应用HTVS筛选到六种BTK抑制剂的BTK研究案例,今天这篇文章主要为大家介绍ROR γ t研究案例。
背景
RAR相关的孤儿受体(RORs)属于细胞内转录因子的核受体家族,由RORα、RORβ和RORγ组成,每种ROR具有多种同亚型。ROR γ t可在先天和适应性免疫系统的多种细胞类型中表达,并驱动Th17细胞分化并诱导细胞因子的转录,包括IL-17A和IL-17F。IL-17A和Th17通路均参与自身免疫疾病的发展,包括系统性红斑狼疮,多发性硬化症,牛皮癣,类风湿性关节炎和克罗恩病。因此,通过小分子结合置换配体结合域(Ligand Binding Domain,LBD)中的内源配体来调节ROR γ t是药物发现研究的一个热点。核受体的配体结合域(LBD)对核定位至关重要,因为它含有激活功能2(Helix 12, H12)区域。在与LBD结合后,小分子效应子诱导H12的构象变化,可以共激活蛋白或共抑制蛋白。在这项研究开展的时候,除内源性配体之外没有已知的ROR γ t小分子结合物,因此项目团队的目标是发现用于治疗炎性疾病的新型反向激动剂。
同源模型拮抗剂和激动剂构象
在该项目开展时,没有可获得的ROR γ t 的LBD结构域晶体结构。为了确定同源模型的最佳模板,研究者对核激素受体家族成员的结构和序列进行分析调研,收集可获得的同一家族蛋白代表性的晶体结构,比较分析公共结构域LBD构象的多样性。经对比后,确定最合适的激动剂构象模板是RORα(PDB ID 1N83, 53%相似度),最合适的拮抗剂构象模板是PPARα(PDB ID 1KKQ,26%相似度)。
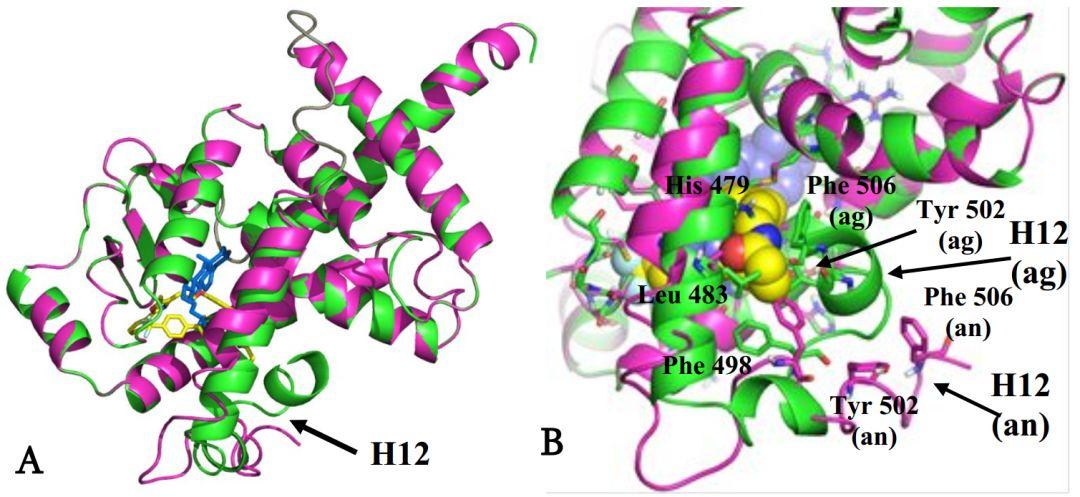
图1. ROR γ t激动剂(绿色)和拮抗剂(紫色)构象的叠合图。激动剂配体(胆固醇)显示为蓝色,拮抗剂配体(GW6471)显示为黄色。(A)蛋白整体结构,箭头突出显示H12;(B)活性位点的局部显示。标记具有显著构象差异的氨基酸GW6471以填充形式显示。Ag:激动剂构象;An:拮抗剂构象。
通过HTVS识别多种活性化合物
研究者应用ROR γ t激动剂和拮抗剂的模建模型作为受体,分别对Janssen公司化合物库(约150万种化合物)进行虚拟筛选,同时对对接结果进行约束,保证命中化合物需与蛋白中的氨基酸Arg367或Arg364的胍基产生氢键作用(这个限制是基于对公开可用的RORα共晶结构的研究和识别各种化学系列的重要相互作用来选择的)。对接完成后,保留GlideScore <-8的化合物,并对所获得的化合物进行过滤,如HTS过滤(去除分子量<150和反应性官能团的化合物),得到24,320种拮抗剂化合物和24,065种激动剂化合物。然后通过应用聚类分析方法发现0.45相似性水平下有11,242个聚类结构。最终,在拮抗剂筛选中,获得1757个hits。研究者们对这些hits进行试验验证,最终有65个化合物通过ThermoFluor实验认证,意味着这次实验筛选的成功率为4.1%。这个结果表明同源模型可成功用于鉴定活性化合物。
应用HTVS发现新的实体分子
通过HTVS鉴定的喹啉叔醇,如图2中所示的Compound 6,显示出100nM的结合亲和力(Kd)。这个化合物被该研究团队用作先导化合物,虽然其吡啶环连接了多个氯原子。由于化合物尚未进行优化,HTS和HTVS可能会识别具有不宜做药的初始命中化合物。这些化合物具有很好的活性,需要被研究者进一步改造优化。Compound 6喹啉中心的2位、3位和4位的优化以及进一步的基于结构的药物设计方法,促进了一系列具有改善ROR γ t抑制效力和反向激动作用模式调节剂的发现。
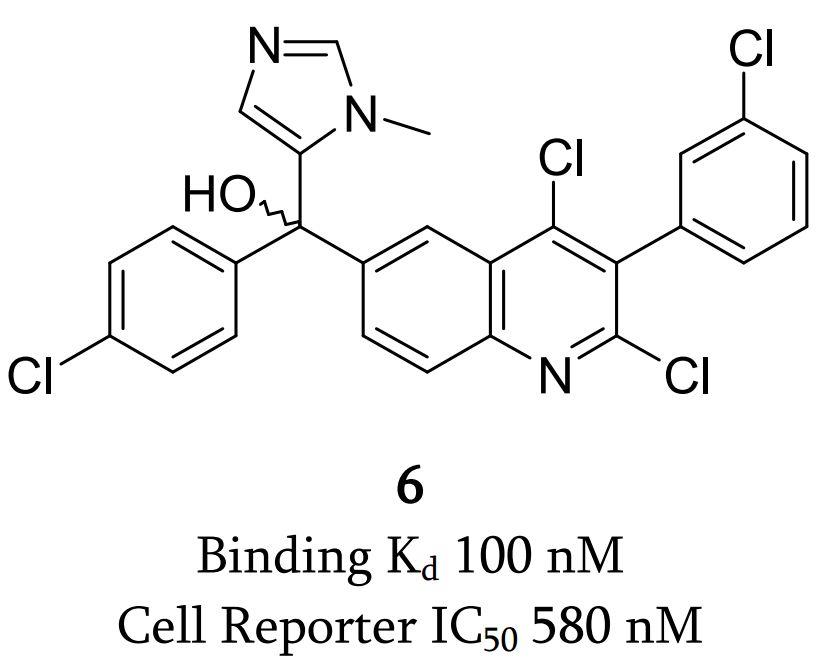
图2.高通量虚拟筛选所获得的Compound 6的结构。
之后研究者解析了Compound 6类似物与人源ROR γ t蛋白LBD结构域复合物的三个高分辨率晶体结构(PDB ID分别为5UFR、5UHI和5UFO),与预测的一致,配体确实占据了疏水性固醇结合口袋。然而, Compound 6在HTVS中预测的结合模式不同于其类似物在晶体结构中的结合模式。激动剂同源性模型与激动剂晶体结构的比较显示三级和二级结构相似(RMSD范围为1.613 Å-1.926 Å)。进一步检查同源模型的LBD内的侧链位置证明了其结合模式之间差异的原由。如图3所示,在激动剂同源性模型中,His323的侧链位于比晶体结构中的位置略高的位置,与配体占据的位置重叠。因此,导致His323和配体之间会存在空间排斥,迫使配体呈现不同的结合模式。尽管Compound 6的预测结合模式与实验所确定的其类似物的结合模式有很大差别,但它在HTVS中仍然具有较好的打分,被包含在ROR γ t确认分析命中列表中。这个案例强调了应尽量使用蛋白可得到的多种构象进行筛选分析。
分子动力学模拟(MD)模拟现在可以以极快的速度在GPU上运行,目前认为比较好的做法是在同源模型基础上运行MD,以获得多个可靠的蛋白构象,之后对多个蛋白结构进行HTVS,以尝试将蛋白质的灵活性结合到筛选中。可惜在这个案例开始时,并没有充足的时间来实施这个想法。
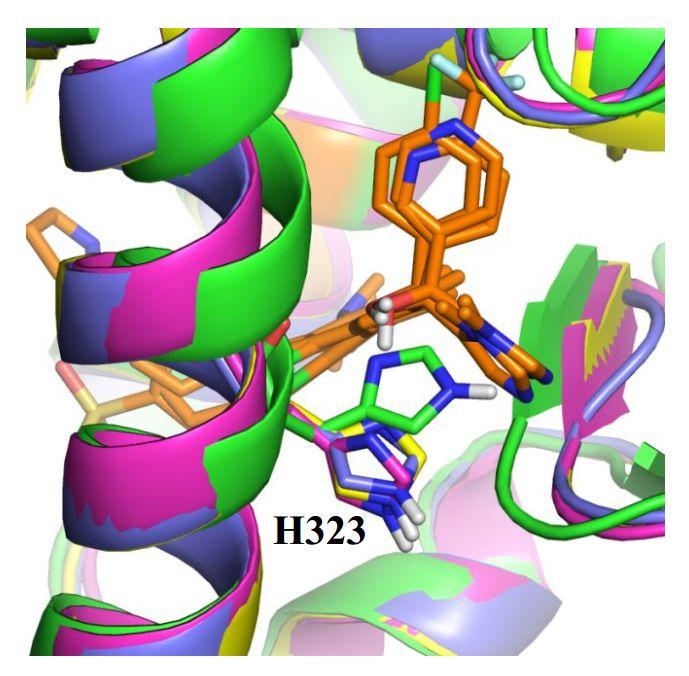
图3. 激动剂同源模型(绿色)和Compound 6类似物-ROR γ t蛋白LBD结构域复合晶体结构的叠合图。PDB ID:5UFR(黄色)、5UHI(蓝色)和5UFO(粉色)。
在这个案例中,研究人员应用同源模建构建了ROR γ t受体结构,通过高通量虚拟筛选获得先导化合物Compound 6,之后对Compound 6进行优化设计,获得与人源ROR γ t具有高亲和力的反向激动剂,该激动剂被定义为新分子实体(New Molecular Entity,NME)。尽管有不确定性存在,但同源模建仍然是晶体结构构建的可替代方法,HTVS并不会因为受体没有晶体结构同源模建而降低筛选活性分子的成功率。
敬请期待案例(三)……
文章来源:
Kelly L. Damm-Ganamet, Nidhi Arora, Stephane Becart, et. “Accelerating Lead Identification by High Throughput Virtual Screening: Prospective Case Studies from the Pharmaceutical Industry” Journal of Chemical Information and Modeling (2019).