引言
今天给大家分享期刊Drug Discovery Today (DDT), Journal of Chemical Information and Modeling (JCIM)、Journal of Medicinal Chemistry (JMC)和Journal of Chemical Theory and Computation (JCTC)在药物发现和药物设计等方法学方面的一些前沿动态,供大家参考。以后我们也会在每周五定时推出各类期刊在生物计算方面的前沿动态,敬请大家期待。
Drug Discovery Today | SARS-COV-2药物高通量筛选的现状及发展方向
主要内容
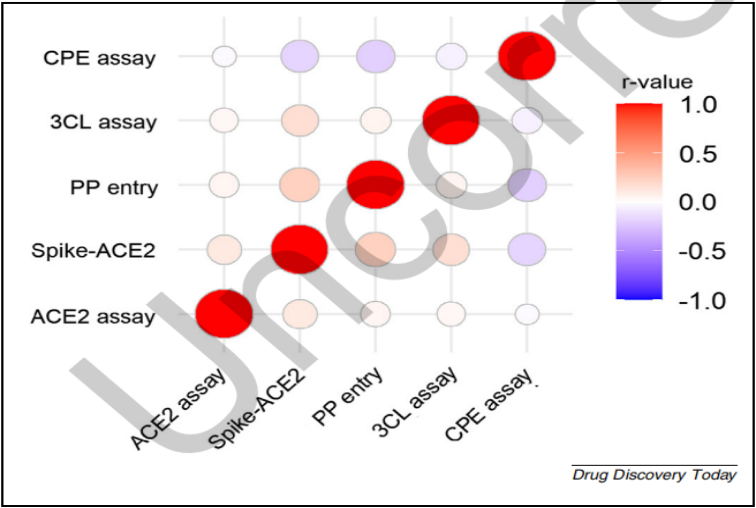
目前新冠疫情仍在继续,为了应对目前的COVID-19大流行,美国国家转化科学发展中心临床前创新部(NCATS)的Xu等人于2021年5月在Drug Discovery Today上发表了名为High-Throughput Screening Assays for SARS-CoV-2 Drug Development: Current Status and Future Directions的研究成果,开发了一组新的分析方法,并通过该方法对具有抗SARS-CoV-2作用的已批准和临床试验药物进行了定量的高通量筛选。
该篇综述将目标特异性分析的复合筛选结果与表型分析的复合筛选结果进行了比较,并应用数据驱动方法评估了每种检测方法识别抗SARS-CoV-2的能力及各种检测方法的优缺点。结果表明多靶点分析在准确性和效率方面优于单靶点分析,而靶点特异性分析更适合研究化合物的作用机制。因此,开发同时针对SARS-CoV-2生命周期中多个靶点的新型HTS检测方法将有助于抗COVID-19药物的发现。
推荐理由
基于本综述提出的SARS-COV-2药物高通量筛选的现状及发展方向得出的筛选经验及比较结果可以为COVID-19药物的筛选分析及研发提供经验。
参考文献
Tuan Xu, Wei Zheng, and Ruili Huang, High-Throughput Screening Assays for SARS-CoV-2 Drug Development: Current Status and Future Directions, Drug Discovery Today, 2021, In Press. DOI:10.1016/j.drudis.2021.05.012.
原文链接
https://doi.org/10.1016/j.drudis.2021.05.012
JCIM | 药物发现及应用中的量子机器学习算法
主要内容
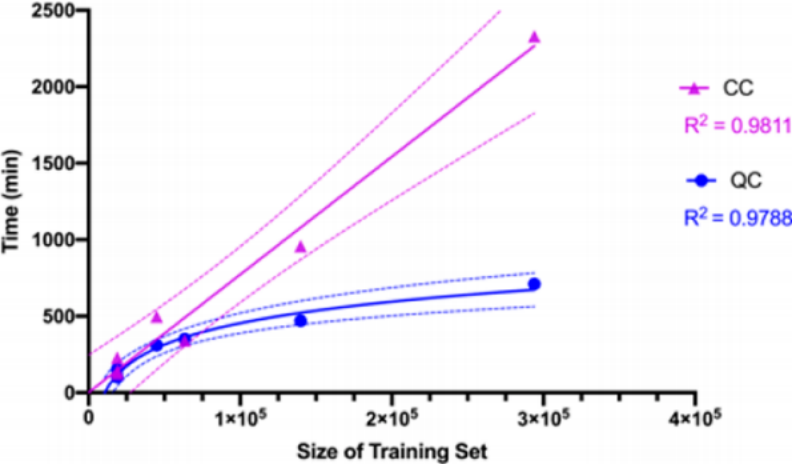
随着机器学习的发展,出现了越来越多的生物靶点小分子及生物体相关数据库,这为药物发现提供了大量的相关数据。但常用的机器学习算法如SVM和DNN等在应用于具有数千个分子体系的大型数据时计算成本十分昂贵,需要克服的挑战之一便是对大量的分子信息进行压缩。因此来自美国合作制药公司的Ekins等人于2021年5月在JCIM上发表了名为Quantum Machine Learning Algorithms for Drug Discovery Applications的研究成果,提出了一种量子计算机(QC)算法,并展示了具体的压缩操作方法。
此外还讨论了不同分子信息的压缩方法及其组合,结果表明QC方法相比于经典计算机(CC)算法具有效率高和成本低的特点。
推荐理由
相比于传统的CC方法,QC方法不随时间尺度呈线性增长,提高了计算效率。随着量子机器学习的发展,QC的应用将大大增加药物数据库的信息规模,为药物发现提供帮助。
参考文献
Kushal Batra, Kimberley M. Zorn, Daniel H. Foil, Eni Minerali, Victor O. Gawriljuk, Thomas R. Lane, and Sean Ekins, Quantum Machine Learning Algorithms for Drug Discovery Applications, Journal of Chemical Information and Modeling, 2021, ASAP. DOI: 10.1021/acs.jcim.1c00166.
原文链接
https://doi.org/10.1021/acs.jcim.1c00166
JMC | 可同时降解EGFR和PARP的双PROTAC分子的设计
主要内容
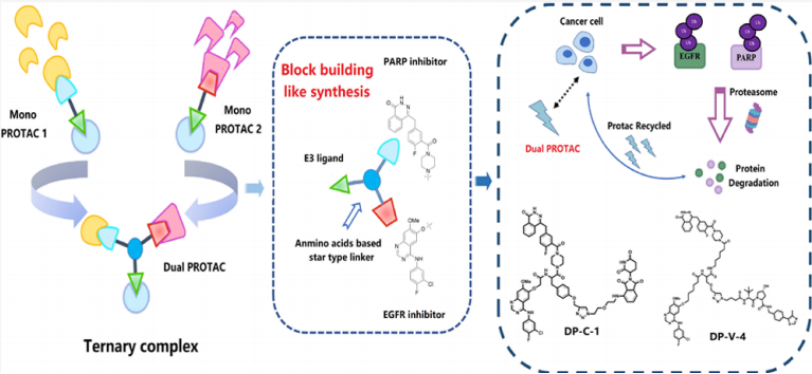
双靶向药物,特别是双特异性抗体药物的研发已经取得了卓越的研究成果,基于上述启发,来自华中科技大学同济医学院与重点实验室的Zheng等人于2021年5月在JMC上发表了名为Rational Design and Synthesis of Novel Dual PROTACs for Simultaneous Degradation of EGFR and PARP的研究成果。将蛋白水解靶向嵌合体(PROTAC)和双靶向的概念结合起来,设计合成了可同时降解EGFR和PARP的双PROTAC分子,并合理地设计及建立了一个新的双靶向PROTAC分子库,并利用收敛合成策略实现了高合成效率。
推荐理由
该研究设计并合成了第一个具有两种不同弹头的双靶向PROTAC分子,并实现了肿瘤细胞中一个小分子同时降解两种完全不同类型的靶蛋白的过程。相信未来这项技术可以大大扩大PROTAC技术的应用,并开辟一个新的药物发现领域。
参考文献
Mengzhu Zheng, Junfeng Huo, Xiaoxia Gu, Yali Wang, Canrong Wu, Qingzhe Zhang, Wang Wang, Yang Liu, Yu Liu, Xuechen Zhou, and Lixia Chen, Yirong Zhou*, and Hua Li, Rational Design and Synthesis of Novel Dual PROTACs for Simultaneous Degradation of EGFR and PARP, Journal of Medicinal Chemistry, 2021, ASAP. DOI:10.1021/acs.jmedchem.1c00649.
原文链接
https://doi.org/10.1021/acs.jmedchem.1c00649
JMC | 咖啡因的药物化学研究
主要内容
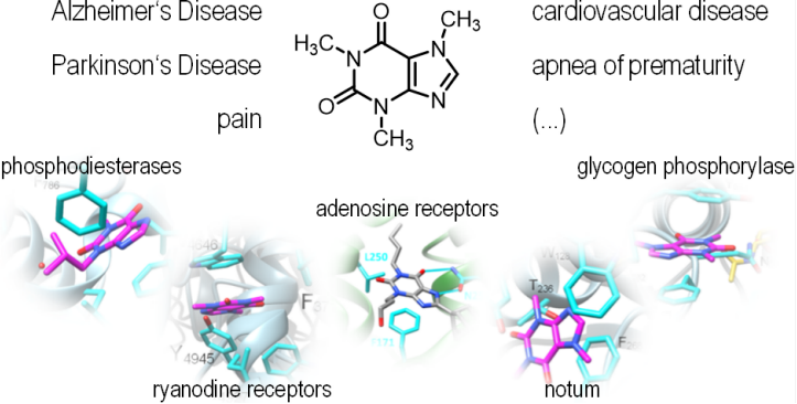
嘌呤生物碱咖啡因是世界上应用最广泛的精神兴奋剂药物,具有多种有益的药理活性。尽管对于咖啡因分子靶点的研究已有几十年的历史,但对咖啡因药理作用的机制理解并不明确。因此许多药物化学项目应运而生,新的蛋白质相互作用不断被发现。2021年5月法兰克福歌德大学药化学研究所联合众药物研究所在JMC上发表了名为The Medicinal Chemistry of Caffeine的综述,该文章介绍了已证实的蛋白质相互作用、结构活性关系和咖啡因的化学生物学的知识。
此外,该文章阐述了咖啡因在受体和酶上分子活性的多样性及促进神经保护作用的几种机制间的复杂相互作用,并强调了新的靶点是药物发现的重要因素。
推荐理由
尽管咖啡因几十年来一直是生命科学的焦点,但咖啡因的未知分子靶点也不断被发现,从而增加了咖啡因的未知药用机制。该文章的相关介绍可以为探索咖啡因的新靶点及作用机制提供帮助。
参考文献
Giuseppe Faudone, Silvia Arifi, and Daniel Merk, The Medicinal Chemistry of Caffeine, Journal of Medicinal Chemistry, 2021, ASAP. DOI:10.1021/acs.jmedchem.1c00261.
原文链接
https://doi.org/10.1021/acs.jmedchem.1c00261
JCTC | 辅助限制脚手架变换模型精确计算结合自由能
主要内容
靶点-药物相互作用的虚拟筛选一直以来都是药物发现过程的一个关键部分。药物化学家通常通过改变环的结构来改变药物支架,从而提高候选药物的结合亲和力并增强候选药物的有利性质。这一过程通常被称为支架跳变。虽然相对结合自由能(RBFE)计算已经成功地预测了结合亲和力的变化,但RBFE计算在支架跳变建模中的应用相对有限,因为该过程涉及到键相互作用,通过计算建模预测该过程十分具有挑战性。为此,2021年5月深圳景泰科技公司联合罗格斯大学综合蛋白质组学研究中心提出了一种处理环开闭收缩膨胀和连接器收缩膨胀的新方法。该方法使用辅助约束限制,在键的断裂和形成过程中,将原子固定在键的末端。
基于大量的化合物,证明了该方法的广泛适用性及较高的精度。此外通过与标准模拟结果的比较,该方法的严格性及准确度也得到了很好的验证。
推荐理由
该研究提出了一种在RBFE计算中处理支架跳跃变换的新方法。该方法依赖于辅助约束,有效防止键断裂形成过程中极端键距的采样。此外,该方法可以使用现有的MD代码而无需修改。该方法有望扩大RBFE计算在药物发现和蛋白质表征过程中的影响并提高其适用性。
参考文献
Junjie Zou, Zhipeng Li, Shuai Liu, Chunwang Peng, Dong Fang, Xiao Wan, Zhixiong Lin, Tai-Sung Lee, Daniel P. Raleigh, Mingjun Yang, and Carlos Simmerling, Scaffold Hopping Transformations Using Auxiliary Restraints for Calculating Accurate Relative Binding Free Energies, Journal of Chemical Theory and Computation, 2021, ASAP. DOI:10.1021/acs.jctc.1c00214.
原文链接
https://doi.org/10.1021/acs.jctc.1c00214