抗体药物作为21世纪主要的治疗方式,其研发过程中的“人源化”是关键步骤之一。传统方法通过最大化人类可变区(V-region)与原始遗传系列的同源性来保持结合力,但往往忽略了分子固有属性的重要性。
Boehringer Ingelheim的研究团队提出了一种新理念:Matrixed CDR嫁接,通过将小鼠抗LAG3抗体的CDRs嫁接到多个不同的人类VH和VL框架区域,评估了表达、亲和力、可开发性和功能等多方面的影响。
图1. 该项研究文章截图
研究内容
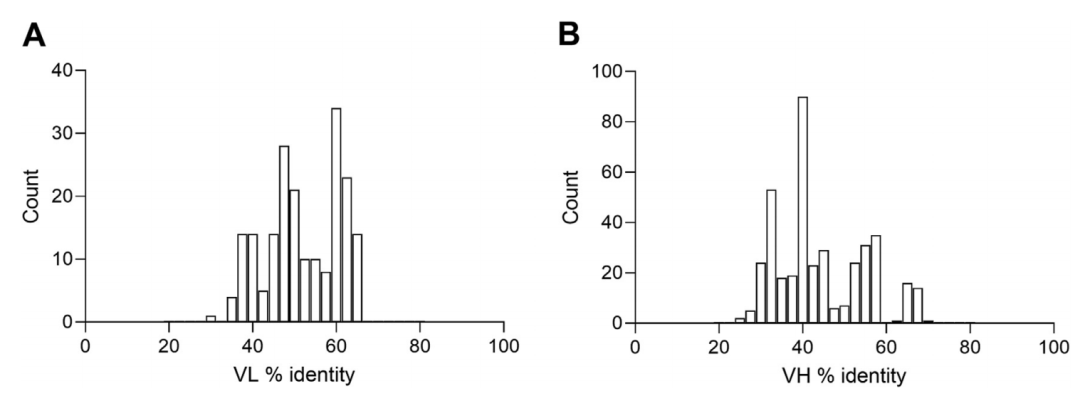
研究团队选择了一个抗LAG3的小鼠单克隆抗体,通过与人免疫球蛋白germlines的同源性比较,查找与抗LAG3抗体V-region同源性最高的人类遗传基因,作为CDR嫁接框架。
图2. 抗LAG3抗体V-region与人免疫球蛋白germlines同源性比较
之后将抗LAG3抗体的CDRs嫁接到14种不同的人类VL和15种不同的VH框架上,形成了210种不同的抗体组合。通过高通量系统,对这些抗体在表达、亲和力、可开发性和功能等方面的表现进行了全面评估。
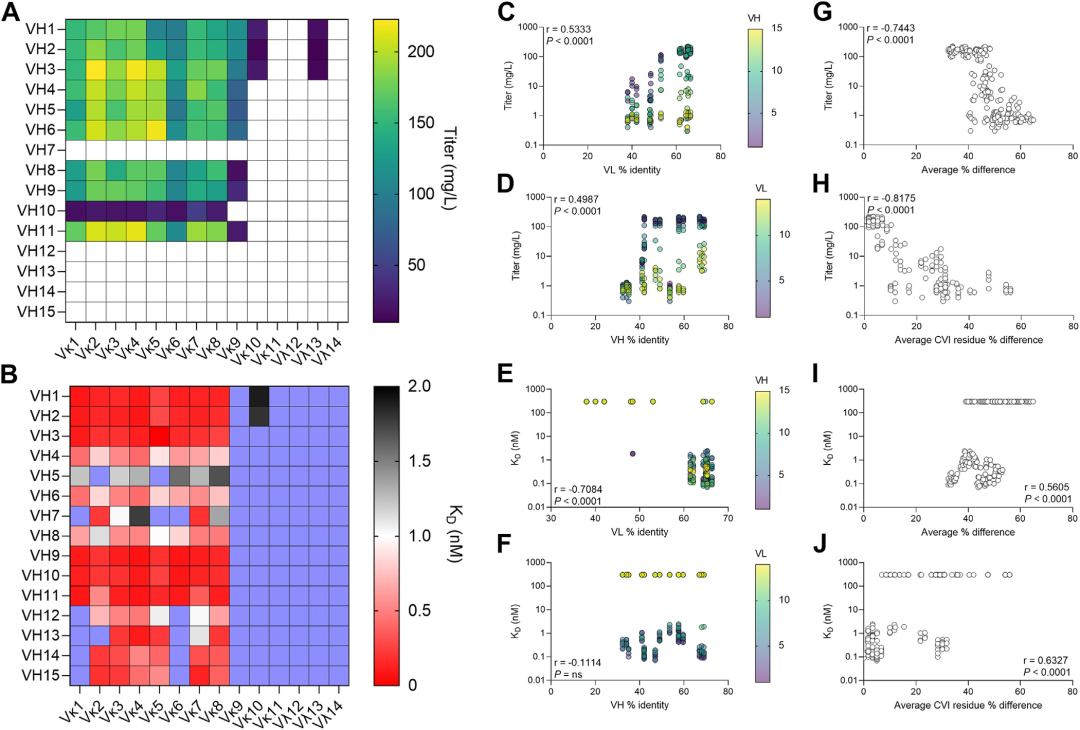
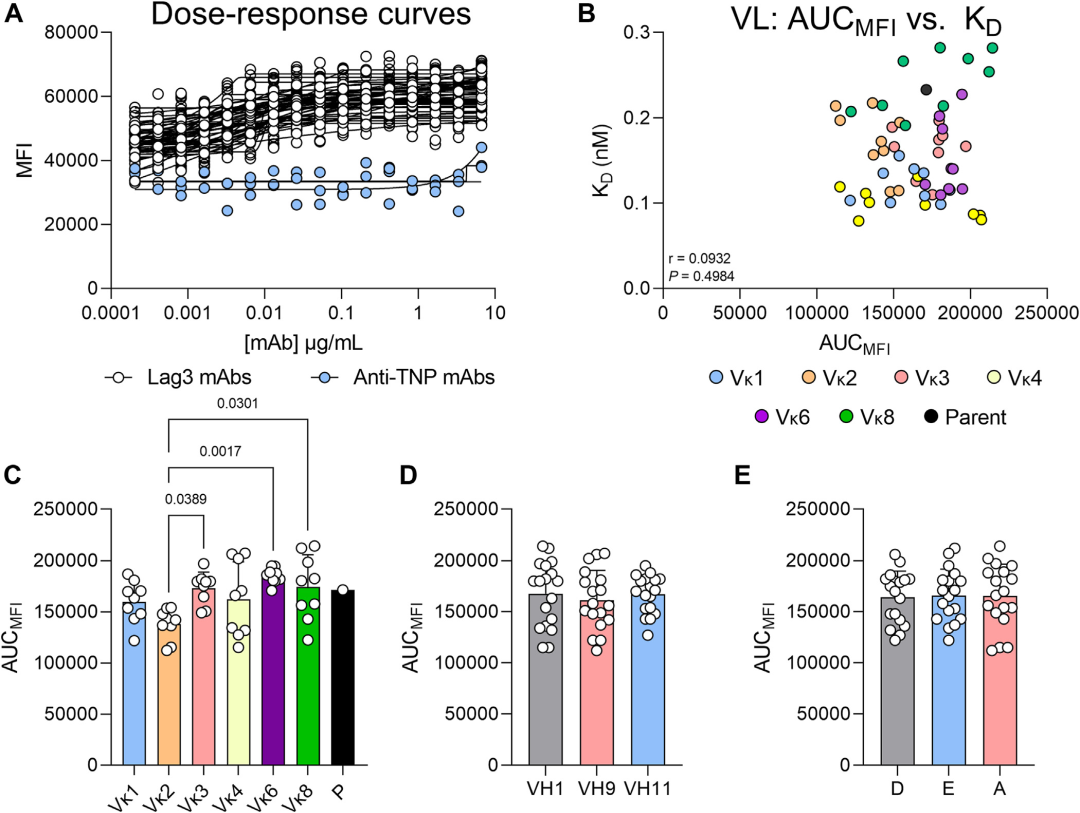
实验结果显示,与抗LAG3抗体序列同源性更高的嫁接体展现出更好的表达量以及对LAG3的亲和力。同源性最低的VL嫁接体其表达和熔点表现最差,而同源性最低的VH嫁接体其纯度结果最差。综合这些实验数据,实验人员挑选了轻链Vκ1、Vκ2、Vκ3、Vκ4、Vκ6和Vκ8以及重链VH1、VH9和VH11,组合成18种抗体分子进行下一步的研究。
图3. 抗LAG3抗体嫁接体的表达量和亲和力。与亲本抗体序列同源性更高的嫁接体展现出更好的表达量和对LAG3的亲和力
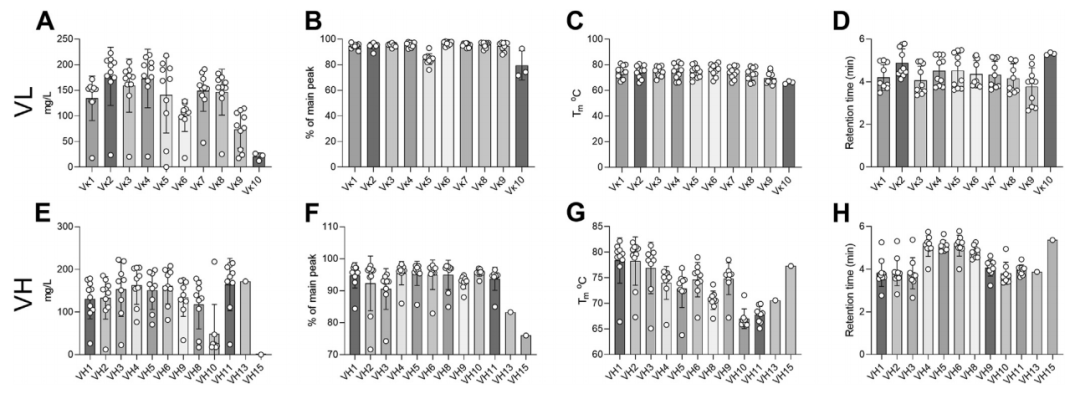
图4. 抗LAG3抗体嫁接体的可开发性数据,包括表达量(A和E)、纯度(B和F)、熔点(Tm, C和G)和亲水性(D和H)。同源性最低的VL嫁接体其表达和熔点表现最差,而同源性最低的VH嫁接体其纯度结果最差
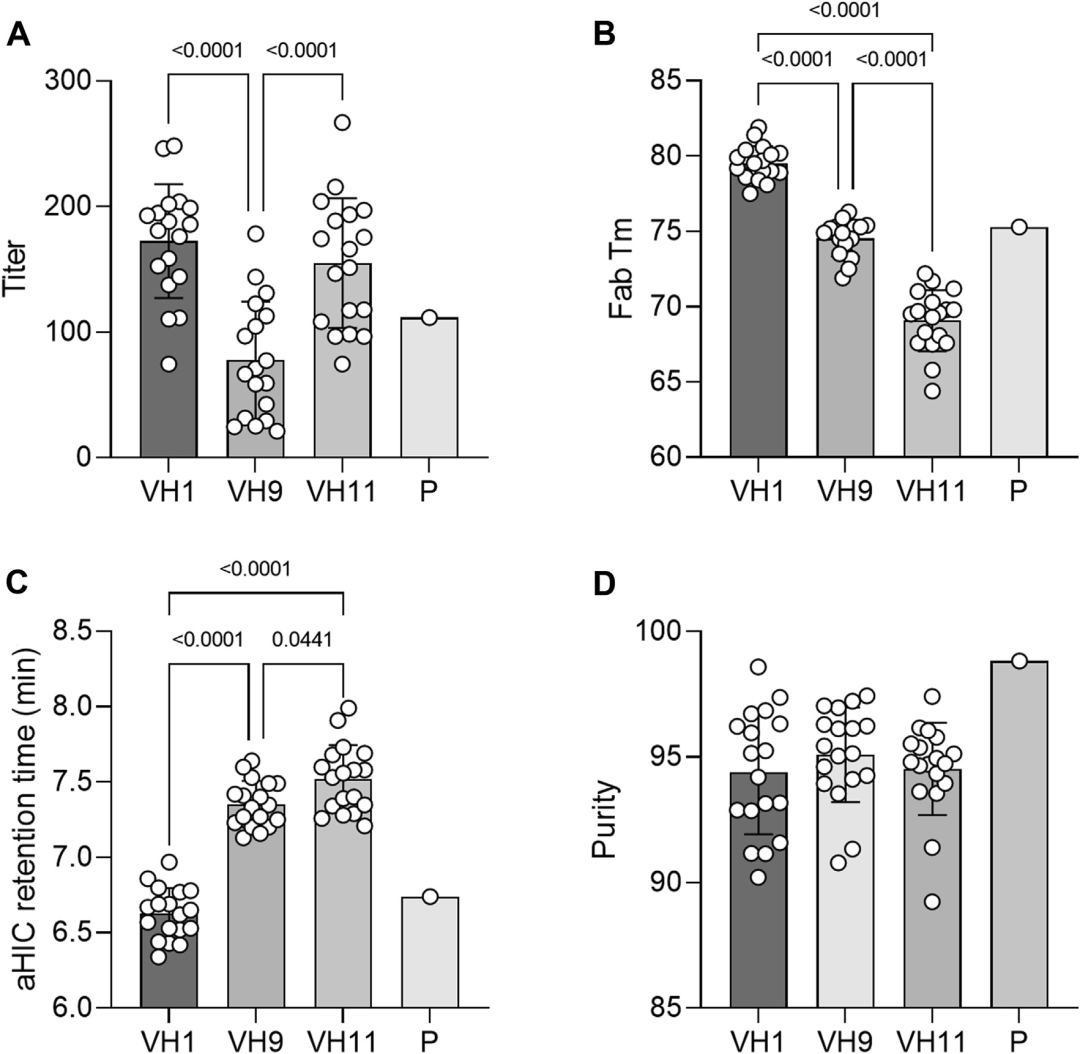
研究员首先对选定的研究嫁接分子进行了工程化调整优化(天冬氨酸异构化位点优化以及潜在脱酰胺化位点优化),并进行亲和力和可开发性评估。结果显示VH框架显著影响表达、稳定性和疏水性,但不影响纯度。同时还评估了嫁接分子对细胞相关LAG3的结合能力。结果显示所有嫁接物均能结合LAG3表达的CHO-K1细胞。
图6. 嫁接分子对细胞相关LAG3的结合能力评估
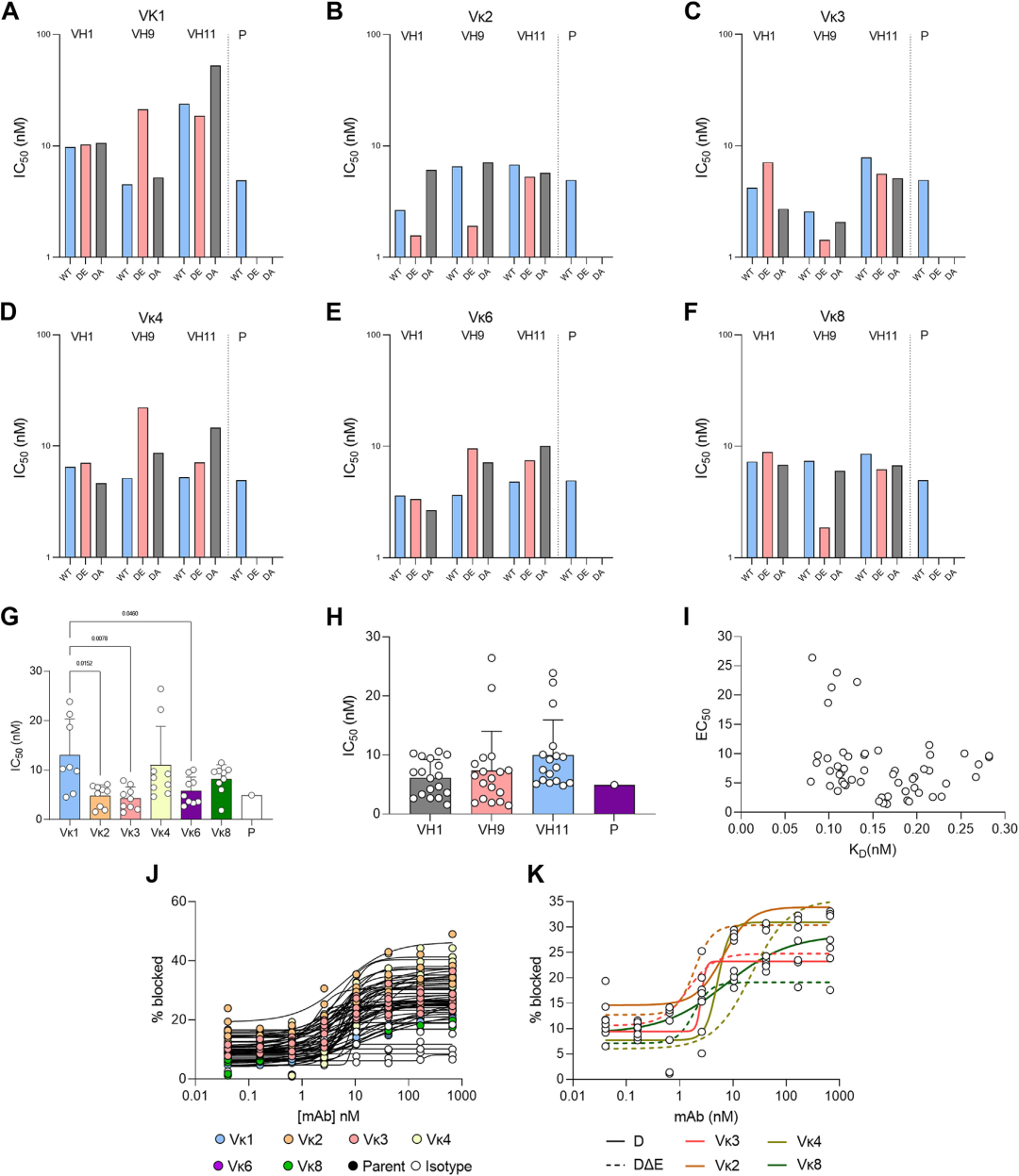
亲本抗LAG3抗体旨在阻断LAG3与MHCII的相互作用。为了评估嫁接分子是否表现出这种LAG3-MHCII阻断功能,研究员对所挑选的嫁接体进一步研究。结果发现,所有嫁接体表现出了阻断活性,与抗体亲和力之间没有显著相关性。
图7. 不同嫁接分子阻断LAG3与MHCII相互作用的能力
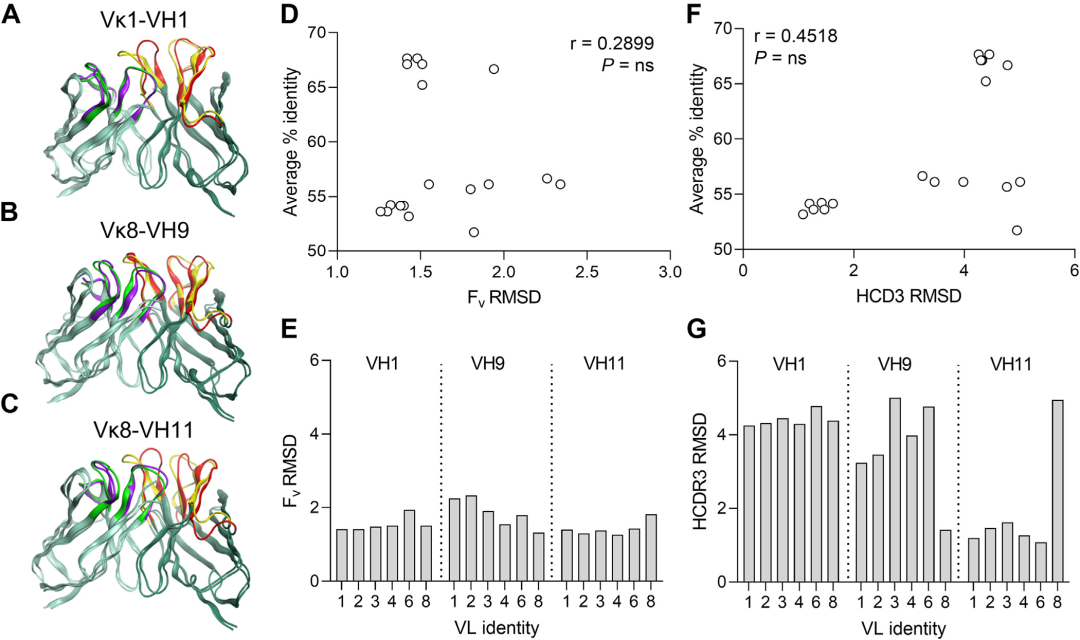
之后研究员将嫁接分子结构与亲本结构进行比较分析。将预测的嫁接分子结构模型与亲本抗LAG3抗体模型496G6的结构进行叠合分析,并计算了嫁接分子不同区域相对于亲本的RMSD值,以评估结构的相似性。通过对抗体的Fv部分和HCDR3的结构模型进行分析,发现一些低同源性的VH嫁接体在HCDR3环的结构中表现出较低的RMSD值,说明结构相似性并不总是与序列同源性直接相关。
图8. 不同抗LAG3抗体嫁接体结构分析
研究结论
VH和VL的影响:研究发现VH框架对抗体的表达、稳定性和亲水性有显著影响,而VL框架则对亲和力、目标结合和功能特性有显著影响。
亲和力与功能:研究指出,亲和力虽然是选择抗体候选物的重要标准,但与功能的相关性并不总是线性的,有些高亲和力的抗体功能表现并不理想。
人源化与开发性:通过Matrixed CDR嫁接方法,研究团队能够识别出在保持或改善亲和力的同时,具有更好开发性特性的抗体。
选择更好的候选物:研究最终表明,通过更广泛的人类框架同源性空间探索,可以找到比最同源的VH/VL对更优的候选抗体,这些候选抗体具有更好的全局属性,可能更快地通过开发阶段,并具有更高的成功概率。
意义与展望
这项研究展示了如何通过现代高通量系统,实现对抗体人源化的更全面、定制化和系统性分析,从而加速发现具有改善全局属性的人源化抗体,提高临床开发的成功率。
不愧是MNC,很系统的研究,信息量很大。局限性在于只涉及了LAG3一个靶点,也未考虑回复突变的影响,后者却是至关重要的。
瑕不掩瑜,文章结论与我们在大量抗体设计项目中的经验是基本一致的,甚至不同germline来源的FR模板的替换可应用在包括人源化在内的多种抗体优化场景中。
文章的计算部分都可以用WeMol实现,使用WeMol的人源化设计功能可以同时评价除了同源性以外的理化性质指标,并轻松指定不同germline的多组FR模板,并批量预测最终人源化变体的结构及计算CDR区的RMSD,实现高通量、高质量、高灵活度的设计。
参考文献:J. Biol. Chem. (2024) 300(1) 10555
Wecomput(唯信计算)致力于”计算技术驱动创新药研发”,基于对创新药物研发流程的深刻理解,融合人工智能、生物物理、高性能计算等技术,打造了独具特色的自动化、智能化、数字化的药物分子生成、设计与模拟平台,有望革新传统药物发现方式,驱动小分子、蛋白质、抗体、mRNA等创新药物的研发进程。核心团队成员来自国际知名AI制药公司、头部药企、知名互联网公司、985高校,在制药、生命科学、人工智能、软件开发等交叉领域有丰富的经验、深刻的理解和饱满的热情。
母公司北京中大唯信科技有限公司于2015年注册成立,入选国家高新技术企业,2021年获红杉资本股权投资,并入选NVIDIA Inception计划资深会员。至今,Wecomput已服务海内外数百家客户,涵盖众多生物医药企业、高校、医院、科研机构,并倾力打造了自主知识产权的分子数字化智能计算平台WeMol。欲了解更多信息,请访问官网www.wecomput.com,或关注公众号“唯信wecomput”。
WeMol(wemol.wecomput.com)是Wecomput开发的面向生物制药、材料、化学等领域的新一代分子数字化智能计算平台,集成了计算生物学、人工智能、量子化学等领域的上百种Wecomput自研及开源的计算与可视化模块,核心算法的速度、准确度超过或媲美国外主流商业软件,尤其特色的抗体人源化设计、蛋白质免疫原性预测、虚拟亲和力成熟、高通量虚拟筛选、RNA序列设计等算法已在多家知名药企的数十个药物发现项目中得到验证和广泛应用。WeMol基于先进的流式架构,可将复杂计算流程简单化、自动化,并支持低代码定制开发和灵活扩展,是业界首款同时面向计算科学家及非计算专业的湿实验人员,旨在构建一个简单、易用、智能、可扩展、可追溯、可重现的一站式计算平台,全方位覆盖大分子生物药设计、小分子化合物设计、分子模拟、数据分析等应用场景,可对Hit->Lead->PCC各阶段进行全链条赋能。发布至今,WeMol已获得了国内外数百家药企及学术单位的青睐与好评。