
引言
新兴病毒如登革和寨卡等都可以引起大范围的病毒传播。作为绝对寄生体,所有病毒有共同的细胞途径,这为开发广谱抗病毒药提供了靶向宿主因子的可能性。人源DEAD-box RNA解旋酶DDX3X是病毒复制必需但同时对于细胞发育具有重要作用,是抗肿瘤的潜在靶点。因此,开发具有抗病毒但同时不影响宿主细胞发育的高选择性DDX3X抑制剂具有重意义。传统DDX3X抑制剂是针对ATP和RNA结合位点,但是该结合位点抑制剂选择性差。意大利遗传研究所Giovanni Maga团队通过结构和序列比对,发现一个独特的结构域(UM),该结构域与人体其他蛋白序列同源性低,因此靶向该结构域,有望发现靶向DDX3X高选择型抑制剂。
先睹为快
靶点
DDX3X:人源DEAD-box RNA解旋酶(PDB ID:2DB3、2I4I)
数据库
Asinex Gold 和 Platinum数据库(共583040个小分子)
计算方法
同源建模,分子对接
计算软件
Schrödinger Prime、PocketPicker、Schrödinger Glide、Gold (chemscore)
计算流程
Giovanni Maga团队运用同源建模和高通量虚拟筛选相结合的策略发现作用于DDX3X特定结合域的抑制剂。通过使用Prime同源模建及PocketPicker找到潜在结合口袋,接着Glide分子对接初步筛选化合物库Asinex Gold 和Platinum共约58万分子,选择得分较高的约7.5万分子用GOLD再次进行对接得到103个化合物,最终选择10个进行生物活性测试。其中化合物5的IC50值在0.7μM,表明它是一种新的DDX3X抑制剂,对5简单修饰改造后的化合物11~13在微摩尔范围内表现出良好的广谱抗病毒药效且无细胞毒,可作为西尼罗河、登革热治疗的候选药物。
基于结构的虚拟筛选
基于结构的药物设计依赖于高分辨率的结构,Giovanni Maga团队在项目之初并无可用结构,作者使用果蝇vase DEAD-box解旋酶的晶体结构(PDB code:2DB3)作为第一个模板,与人源DDX3X的序列同源性为44%但缺少独特结构域(UM),因此,处于开放构象中的DDX3X晶体结构(PDB code:2I4I)作为第二个模板填补了这个空白,同源建模中的UM与晶体结构中的RMSD为1.03 Å, 建模结果可靠。利用PocketPicker在UM域发现了一个由α螺旋组成的潜在结合口袋。接着使用Glide分子对接初步筛选约58万分子,选择得分较高的约7.5万分子用GOLD再次进行对接得到103个化合物,根据分子结构和与活性位点的极性相互作用,最终选择10个进行生物活性测试。一系列突变实验显示Glu256对DDX3X酶活性至关重要,是抑制剂能否与UM域结合的主要决定因素。活性测试结果表明化合物5及其修饰产物表现出良好的广谱抗病毒药效且无细胞毒,可作为西尼罗河、登革热治疗的候选药物。这首次为开发兼具广谱抗病毒活性和靶标选择性分子提供了理论和实例支撑。
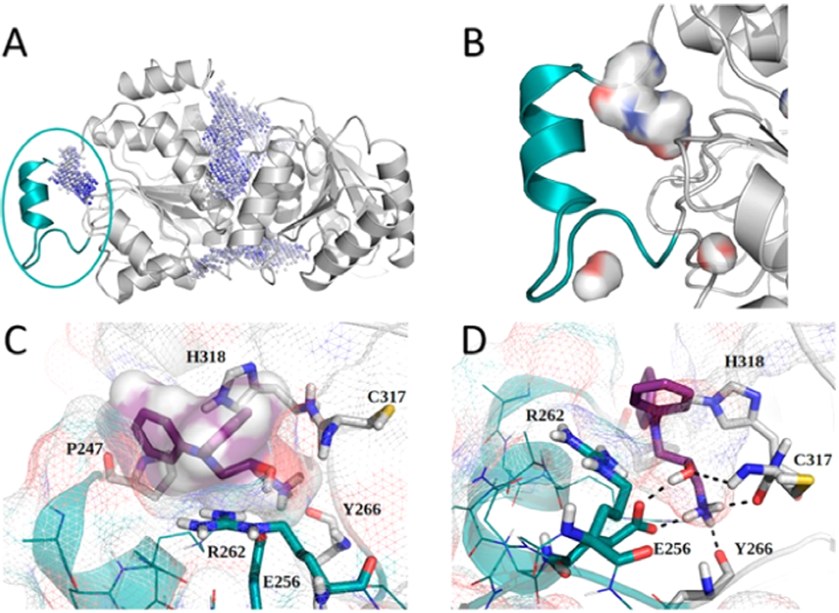
图1. DDX3X抑制剂结合口袋的建模过程.
图片来源:JMC
体外活性验证
生化活性分析显示化合物5活性较好,而化合物1和7对接得分较高却无活性的原因是缺少与5一样和Glu256、Cys317的相互作用。化合物11是5的乙酸盐形式,12和13是11的R和S对映异构体。抗病毒活性测试显示化合物11及其对映异构体12和13能减弱DENV和WNV在Huh-7细胞系上的复制能力,在微摩尔范围内显示出令人鼓舞的抗病毒活性,IC50(DENV)值大致相当,IC50(WNV)甚至比广谱抗病毒药利巴韦林更好,且无明显细胞毒。使用三种RNA解旋酶对化合物11和14进行的抑制试验显示,所有化合物均抑制DDX1,比DDX3X约低4个数量级,且对STRS2和NS3完全无活性,证实了对DDX3X的选择性抑制。
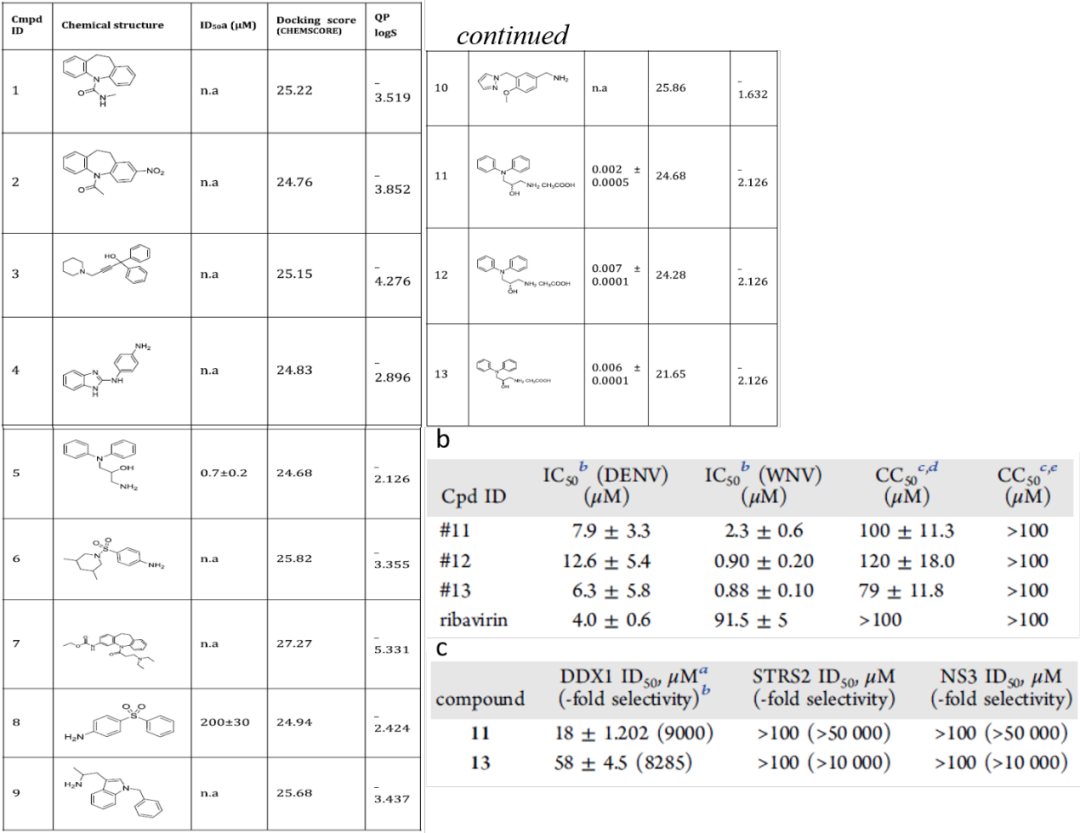
图2. 抑制剂对DENV和WNV的抗病毒活性及对DDX3X的选择性
图片来源:JMC
参考文献
Unique Domain for a Unique Target: Selective Inhibitors of Host Cell DDX3X to Fight Emerging Viruses. Valentina Riva, Anna Garbelli, Annalaura Brai, Federica Casiraghi, Roberta Fazi, Claudia I. Trivisani, Adele Boccuto, Francesco Saladini, Ilaria Vicenti, Francesco Martelli, Maurizio Zazzi,
Simone Giannecchini, Elena Dreassi, Maurizio Botta, and Giovanni Maga*. J. Med.Chem.2020.07.30; doi: https://doi.org/10.1021/acs.jmedchem.0c01039