引言
今天给大家分享期刊Journal of Chemical Information and Modeling (JCIM)、Journal of Medicinal Chemistry (JMC)、Trends in Pharmacological Sciences (TIPS)、Advanced Drug Delivery Reviews (ADDR)和Biomedicine & Pharmacotherapy (BP)在药物发现、药物设计和药物合成等方法学方面的一些前沿动态,供大家参考。以后我们也会在每周五定时推出各类期刊在生物计算方面的前沿动态,敬请大家期待。
JCIM | DeepBSP:一种精确预测蛋白质−配体对接位姿的机器学习方法
主要内容
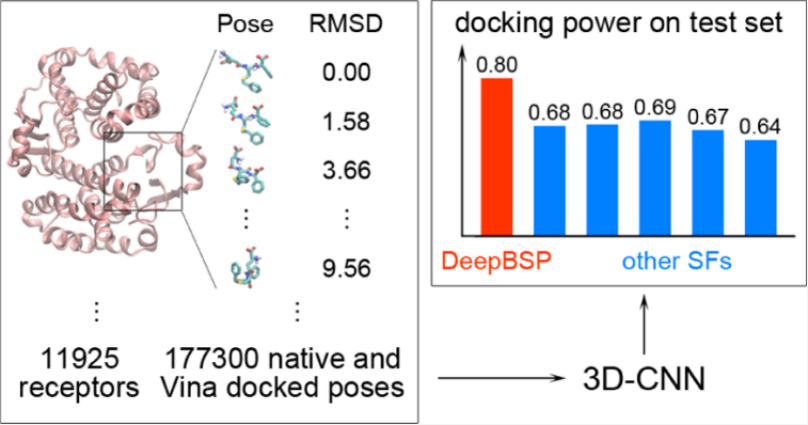
近年来,基于打分功能的机器学习方法显著提高了打分能力,但由于机器学习方法的训练数据集中缺乏不合理结构的信息,造成了其在区分原始的合理结构和对接的不合理结构方面表现不佳。
为此,华东师范大学化学与分子工程学院联合上海分子治疗与新药开发工程研究中心于2021年5月20日在JCIM上发表了名为 DeepBSP:Machine Learning Method for Accurate Prediction of Protein−Ligand Docking Structures的研究成果。开发了一个名为DeepBSP的机器学习模型。该方法可以直接预测配体对接后的构型与其原始构型的均方根偏差(RMSD)。
此外将DeepBSP方法在万级规模的包含初始结构及虚假结构的数据集上进行了训练,并与其他的评分方法进行了对比,结果表明该模型显示出了优秀的对接能力。应用DeepBSP方法可以更准确地预测最接近初始复合物构型的最佳结合位姿。
评论
基于机器学习的DeepBSP-3D-CNN模型,可以根据其原始结合位姿直接预测配体对接位姿的RMSD,相比于以往打分方法预测更准确。期待DeepBSP模型在从对接过程产生的许多对接位姿的准确预测方面能够有良好的应用前景。
参考文献
Jingxiao Bao, Xiao He, and John Z. H. Zhang, DeepBSP:A Machine Learning Method for Accurate Prediction of Protein−Ligand Docking Structures, Journal of Chemical Information and Modeling, 2021, 61, 5, 2231-2240. DOI:10.1021/acs.jcim.1c00334.
原文链接
https://doi.org/10.1021/acs.jcim.1c00334
JMC | 针对蛋白酶活性位点的
共价小分子免疫调节剂
主要内容
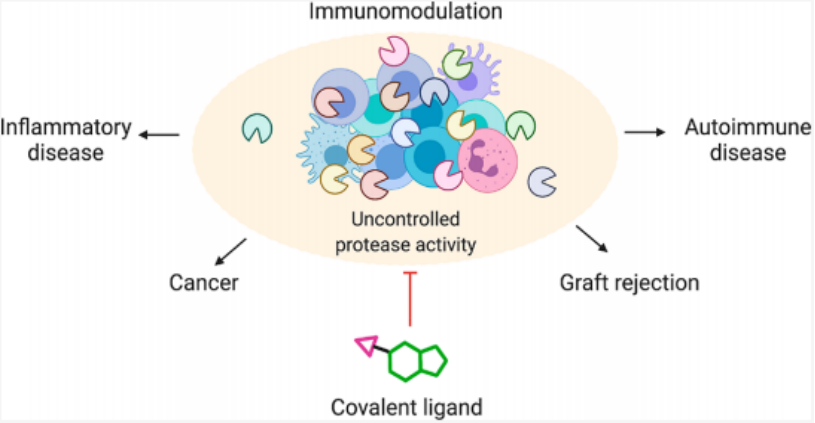
蛋白酶抑制剂可通过共价修饰来改变蛋白质活性从而调节免疫反应,可作为一类重要的药物。2021年4月27日Euna等人在JMC上发表了名为Covalent Small Molecule Immunomodulators Targeting the Protease Active Site的综述。
该文章提供了蛋白酶研究相关技术的概述,重点概述了化学蛋白质组学方法和筛选平台的最新进展以及用来针对免疫调节蛋白酶的共价抑制剂的研究成果。
此外,重点讨论了针对蛋白酶活性位点的共价抑制剂的开发,及蛋白酶抑制剂在基于活性的蛋白质分析、成像探针开发和抑制剂设计中的重要应用。并强调了将蛋白酶抑制剂作为化学免疫调节剂的重要性。
评论
对于蛋白酶抑制剂的开发,实现靶点特异性一直是开发小分子蛋白酶抑制剂的主要挑战,蛋白酶抑制剂开发的另一个主要挑战是清楚地了解蛋白酶执行其生物功能的机制。期待新的化学工具和蛋白质组学方法的出现,能够加速蛋白酶抑制剂的研发,实现化学免疫学领域上的新突破。
参考文献
Hong-Rae Kim, Ravichandra Tagirasa, and Euna Yoo, Covalent Small Molecule Immunomodulators Targeting the Protease Active Site, Journal of Medicinal Chemistry, 2021, 64, 9, 5291-5322. DOI: 10.1021/acs.jmedchem.1c00172.
原文链接
https://doi.org/10.1021/acs.jmedchem.1c00172
TIPS | 基于片段的药物设计
促进选择性激酶抑制剂的发现
主要内容
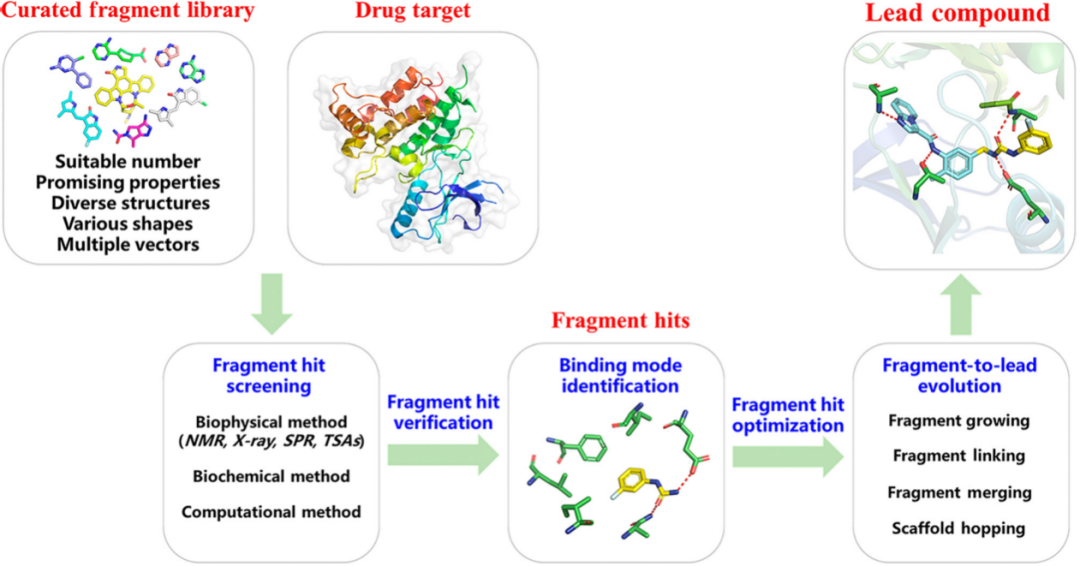
蛋白激酶(PKs)是一种重要的药物靶点,但激酶的选择性是蛋白激酶抑制剂(PKIs)的设计面临的主要挑战。基于片段的药物发现(FBDD)在发现高度特异性的PKIs方面取得了巨大的成功。但与此同时,该方法很难用于复杂的激酶-片段相互作用并且缺乏对这些相互作用的系统讨论。为此Wang等人于2021年5月在Trends in Pharmacological Sciences上发表了名为Fragment-Based Drug Design Facilitates Selective Kinase Inhibitor Discovery的研究成果。介绍了FBDD策略在PKIs设计中的优势,总结和分析了激酶-片段相互作用选择性的关键特征。此外还介绍了一些典型的研究案例,并探索了满足使用FBDD设计选择性PKI的需求。
评论
尽管选择性激酶抑制剂的研究仍存在挑战和障碍,但使用FBDD策略发现选择性PKI已经取得了阶段性的成功,期待未来可以开发出针对不同PK的更多的PKI。
参考文献
Zhi-Zheng Wang, Xing-Xing Shi, Guang-Yi Huang, Ge-Fei Hao, and Guang-Fu Yang, Fragment-Based Drug Design Facilitates Selective Kinase Inhibitor Discovery, Trends in Pharmacological Sciences, 2021, ASAP. DOI: 10.1016/j.tips.2021.04.001.
原文链接
https://doi.org/10.1016/j.tips.2021.04.001
ADDR | 人工智能在3D打印药物方面的应用
主要内容
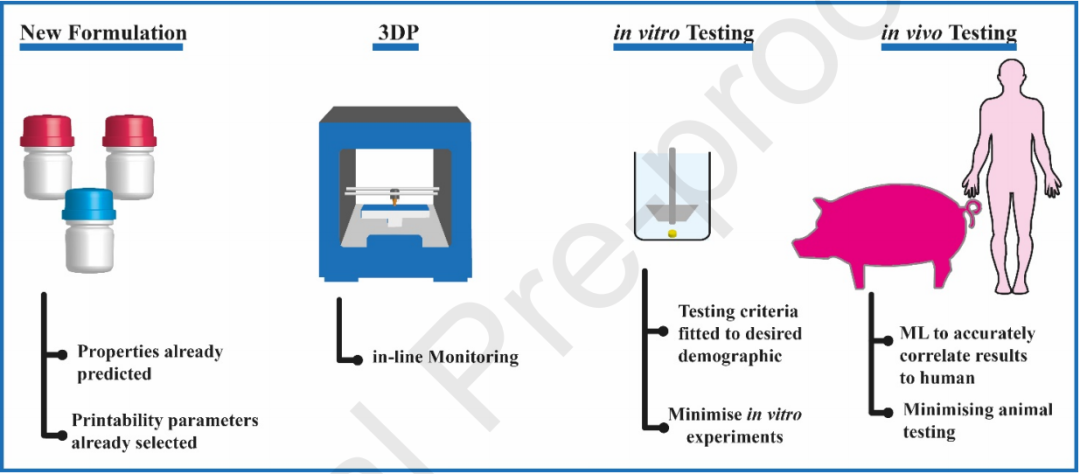
人工智能(AI)正在重新定义我们在这个世界上的存在方式。在社会的几乎每个领域,人工智能都以超人的速度和智力发展着。但对于制药领域还没有真正的使用人工智能。2021年5月15日,Elbadawi等人在Advanced Drug Delivery Reviews上发表了名为Harnessing Artificial Intelligence for the Next Generation of 3D Printed Medicines的研究成果,3D打印(3DP)为按需生产定制药品开辟了一条道路。
因为机器学习可以准确地预测最优过程参数,这使得AI为配方过程提供了无数的选择。该篇综述强调了人工智能如何与医药3DP管道相结合并摆脱其长期以来的“一刀切”药物供应方式,逐步趋向个性化药物的管理。
该文章还表明人工智能还可以被纳入一个制药3DP“物联网”,这些技术将加速临床环境中药物3DP的使用,从而将现在药学推向个性化药学。
评论
医药3DP可提供个性化药物,但缺陷在于需要有经验和知识的3DP从业者的在场。传统工艺优化技术有多种方法,但未能实现充分优化。ML可以提供3DP药物生产的每个阶段的智能优化,从而消除临床采用该技术的障碍。此外,制药3DP的每个阶段都可以构建成智能物联网,智能硬件可以处理开发的每个阶段,此研究成果将消除对人力的需要,从而给予患者可定制的、个性化的药物。
参考文献
Moe Elbadawi, Laura E. McCoubrey, Francesca K. H. Gavins, Jun Jie Ong, Alvaro Goyanes, Simon Gaisford, and Abdul W. Basit, Harnessing Artificial Intelligence for the Next Generation of 3D Printed Medicines, Advanced Drug Delivery Reviews, 2021, In press. DOI: 10.1016/j.addr.2021.05.015.
原文链接
https://doi.org/10.1016/j.addr.2021.05.015
BP | 治疗COVID-19的主要蛋白酶抑制剂:
药物再利用和分子对接
主要内容
目前新冠疫情仍在泛滥,尽管新冠疫苗已经研发并被接种,但仍需一些特效药物来治疗。2021年5月Hasan等人在Biomedicine & Pharmacotherapy上发表了名为Main Protease Inhibitors and Drug Surface Hotspots for the Treatment of COVID-19: A Drug Repurposing and Molecular Docking Approach的研究成果。该文章应用药物再利用和分子对接方法来筛选了已批准的MPP抑制剂及其衍生物,并提出了一种针对COVID-19的特殊治疗药物。
本文采用分子对接技术对靶点药物进行了研究,通过分子动力学确定了对接复合物的结合稳定性,并进行了吸收、分布、代谢和排泄分析,以了解筛选出的MPP抑制剂的药代动力学和药物相似性。该研究结果表明,帕立他普韦及其类似物具有非常好的效果,此外排名前5的预测药物(帕立他普雷韦、格列卡普雷韦、奈菲纳韦和洛匹那韦)在SARS-CoV-2MP蛋白的活性位点表现出良好的构象稳定性。该研究还表明帕立他普雷韦及其类似物可能对SARSCoV-2有效。
评论
帕立他普韦及其类似物可能比其他先前批准的MPP抑制剂更有前途。但该研究成果目前缺乏体内疗效测试。因此,期望通过临床试验可以快速评估帕立他普韦及其类似物的疗效,从而作为新冠病毒治疗候选药品,为新冠患者提供福音。
参考文献
Mahmudul Hasan, Md. Sorwer Alam Parvez, Kazi Faizul Azim, Md. Abdus Shukur Imran, Topu Raihan, Airin Gulshan, Samuel Muhit, Rubaiat Nazneen Akhand, Syed Sayeem Uddin Ahmed, and Md Bashir Uddin, Main Protease Inhibitors and Drug Surface Hotspots for the Treatment of COVID-19: A Drug Repurposing and Molecular Docking Approach, Biomedicine & Pharmacotherapy, 2021, 140, 111742. DOI: 10.1016/j.biopha.2021.111742.
原文链接
https://doi.org/10.1016/j.biopha.2021.111742