
引言
细胞周期蛋白依赖性激酶(CDK)是一类丝氨酸/苏氨酸蛋白激酶,在大多数人类癌症中观察到CDKs的异常激活和/或异常表达,开发CDKs小分子抑制剂已成为一种新的癌症治疗途径。目前已有多种FDA批准的CDK4/6抑制剂,如辉瑞公司的Palbociclib、诺华公司的Ribocilib以及礼来公司的Abemaciclib等。虽然这些药物取得了良好的疗效,但在短期服药后往往会出现抗药性,并不断出现严重的不良反应。目前多靶点小分子的发现已经成为克服靶向疗法耐药性的一种有效策略。而CDK9已被广泛认为是一个潜在的抗肿瘤靶点,其过度表达已被广泛证实有助于CDK4/6抑制剂的耐药性的产生。因此,作者推测同时针对CDK6和9的小分子抑制剂不仅具有协同/相加的抗癌活性,而且可以规避对CDK4/6抑制剂的耐药性。基于此,作者借助分子模拟手段,设计开发了选择性的CDK6/9双抑制剂,提高了疗效,减少了毒副作用,并延缓了耐药现象。
先睹为快
单位与作者
安徽医科大学刘新华教授课题组
研究靶点
细胞周期蛋白依赖性激酶6和9(PDB ID:5L2I和6GZH)
数据库
药物合成方法合成的59个化合物
计算方法
分子对接
计算软件
Discovery Studio 2017 R2
计算流程
作者首先采用酶活性测定方法对实验室现有化合物库进行了筛选,发现了对CDK6/9具有中等抑制活性的先导化合物8。随后,借助分子对接方法揭示了化合物8分别与CDK6和9的结合模式,并对比了该结合模式与共晶化合物的差异。基于对复合物模型的观察,并结合SAR研究,作者对化合物8进行了逐步结构改造,最终发现了化合物66为最有效的CDK6/9双靶点抑制剂,对这两个靶标具有平衡的效力,并且对CDK2具有良好的选择性。生物学研究表明,化合物66直接与CDK6/9结合,效力为化合物8的百倍以上,IC50值分别为0.0405和0.0395μM,该CDK6/9双靶点抑制剂在肿瘤治疗中具有巨大的潜力。
先导化合物的发现
为了寻找有效的CDK6和CDK9双重抑制剂,作者通过酶活性测定对实验室现有化合物数据库进行了筛选。初步确定了一种嘧啶二胺类(化合物8)具有对CDK6和CDK9的中度抑制作用(IC50:3.43~6.65μM),对CDK2具有很强的抑制作用(IC50:0.031 μM)。因此,化合物8可作为开发CDK6和CDK9双重抑制剂的良好先导化合物。为了改善和平衡CDK6/9的活性,提高对CDK2的选择性,作者通过基于受体结构的药物设计和QSAR研究方法,对化合物8进行了下一步优化。
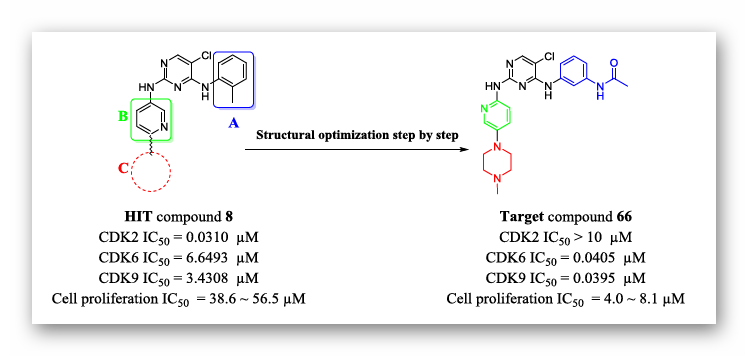
图1. 结构改造提升化合物8的活性
图片来源JMC
先导化合物与CDK6/9的结合模式
作者基于CDK6-Palbociclib和CDK9-A86的复合物结构,通过Discovery Studio 2017 R2中的ZDOCK模块对化合物8与CDK6、9分别进行了对接,阐明了其结合模式与共晶化合物的差异。从对接模型中,观察到化合物8与CDK6或CDK9之间的关键相互作用类似于Palbociclib或A86,其中2-氨基嘧啶和CDK6的关键残基Val101、CDK9的关键残基Cys106形成氢键。化合物8的邻甲基苯基与Palbociclib的环戊基和A89的环丙基相似,占据了CDK6的Val27、Ile19和Asn150或CDK9的Val33、Ile25和Phe30形成的疏水口袋,但化合物8不与CDK6的亲水区相互作用。另外,CDK9还具有由Asp167和Lys48形成的亲水区。然而,几乎没有已知的CDK9抑制剂占据这个区域。Palbociclib的哌嗪环位于溶剂暴露区域,但对CDK4/6的抑制起关键作用。
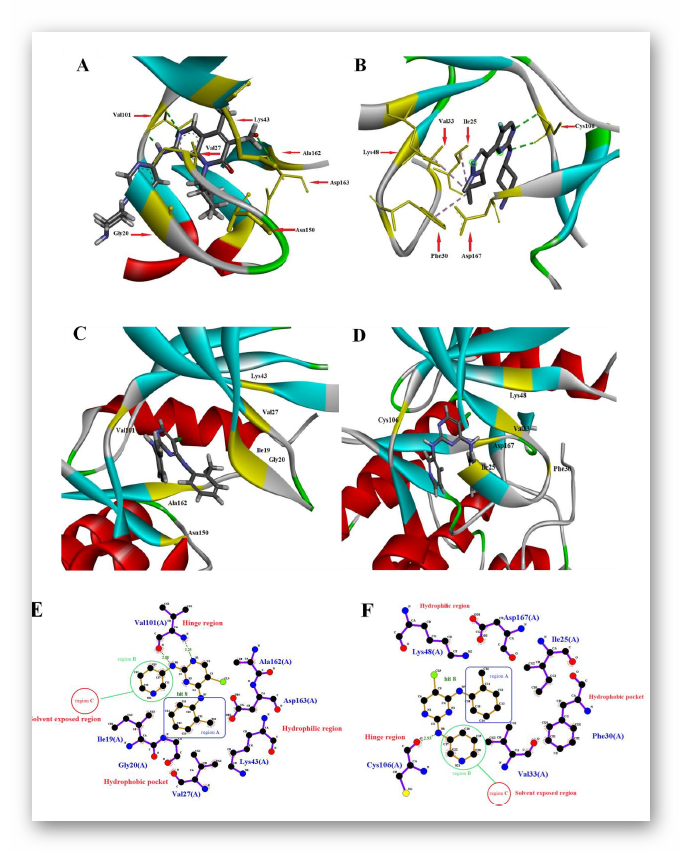
图2. 化合物8及共晶化合物与CDK6/9的结合模式
图片来源JMC
理性设计CDK6/9双靶点抑制剂
基于分子对接结果,作者对化合物8进行了结构改造和SAR研究。为了模拟Palbociclib的哌嗪环,在吡啶环末端引入各种脂肪族杂环结构,从而发现了活性有很大提高的N-甲基哌嗪衍生物。考虑到两个靶标之间的平衡作用,引入乙酰氨基与位于亲水区的关键残基Lys43CDK6/Lys48CDK9和Asp163CDK6/Asp167CDK9相互作用。结果发现了比化合物8效力提高近100倍(CDK6)和170倍(CDK9)的化合物66,其IC50值分别为0.0405和0.0395μM。更重要的是,与Palbociclib和Abemaciclib相比,化合物66对CDK6和9表现出平衡效力,IC50值几乎相等,并且对CDK2具有良好的选择性。
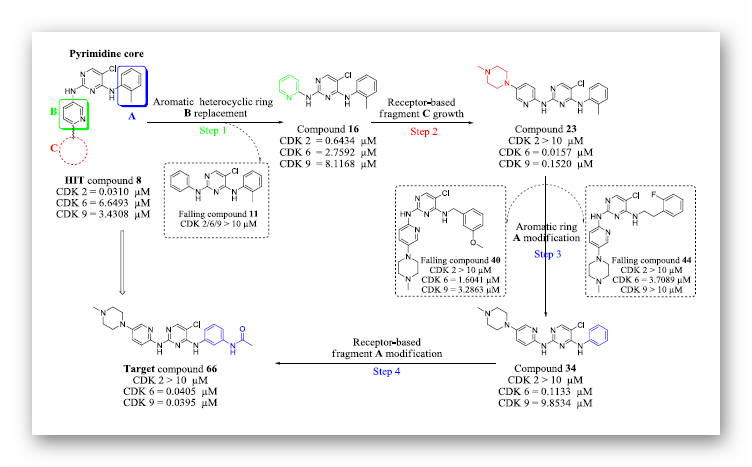
图3.以化合物8为先导化合物进行结构优化
图片来源JMC
活性验证
作者进行生物活性实验研究表明,化合物66直接与CDK6/9结合,通过阻断细胞周期进程和诱导细胞凋亡,抑制其下游信号通路,抑制细胞增殖。重要的是,化合物66在小鼠移植瘤模型中对肿瘤生长有明显的抑制作用,且无明显毒性,表明化合物66在肿瘤治疗中具有广阔的应用前景。因此,上述结果对开发平衡的CDK6/9双靶点抑制剂用于癌症治疗具有重要意义。
参考文献
Wang Y, Chen X, Yan Y, et al. Discovery and SARs of 5-Chloro-N 4-phenyl-N 2-(pyridin-2-yl) pyrimidine-2, 4-diamine Derivatives as Oral Available and Dual CDK 6 and 9 Inhibitors with Potent Antitumor Activity[J]. Journal of Medicinal Chemistry, 2020, 63(6): 3327-3347. DOI: 10.1021/acs.jmedchem.9b02121